在25 ℃时,用石墨电极电解2.0 L 0.5mol·L-1 CuSO4溶液。5min后,在一个石墨电极上有6.4 g Cu生成。试回答下列问题。
(1)发生氧化反应的是__________极,电极反应式为____________。
(2)若电解后溶液的体积不变,则电解后溶液的pH为____________。
(3)若将溶液恢复到与电解前一样,则需加入________mol的_______。
氯水中存在如下平衡:Cl2 +H2O ⇌ HCl+HClO。向氯水中加入下列物质,回答各问题:
(1)加入少量CaCO3(s),发生反应的离子方程式表示为__________________,平衡向________移动(填“正向”、“逆向”或“不”,下同),HClO的浓度______(填“增大”、“减小”或“不变”,下同)。
(2)加入少量NaCl(s),平衡向_________移动,HClO的浓度___________。
(3)加入少量NaOH(s),平衡向__________移动,HClO的浓度____________。
(4)加入少量NaBr溶液,发生反应的离子方程式表示为____,HCl的物质的量_____。
(5)加入少量浓品红试液,实验现象为_____________,HCl的物质的量___________。
(6)加蒸馏水稀释,HClO的浓度__________。
在物理和化学中,有些原理、定律具有相似性。如物理中有机械守恒定律,化学中有质量守恒定律。比较它们有助于我们的学习。
(1)1834年,物理学家楞次(1840年—1865年)概括了各种实验结果,得到如下结论:感应电流具有这样的方向,就是感应电流的磁场总要阻碍引起电流的磁通量变化。这就是楞次定律。请写出与楞次定律相似的化学原理或定律:______________________________;
其内容是_______________________________________________________________________
____________________________________________________________________________。
(2)在物理学的匀变速直线运动中常用图来分析速度、时间和位移相当于如图甲中阴影部分所占的面积。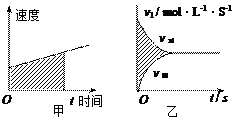
现在容积为2L的密闭容器中进行某一可逆反应: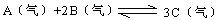 ,其中B物质的正反应速率
,其中B物质的正反应速率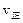 逆反应速率
逆反应速率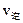 随时间变化的关系如右图乙所示,则图中阴影部分的面积表示的意义为:___________________
随时间变化的关系如右图乙所示,则图中阴影部分的面积表示的意义为:___________________
已知Cu(OH)2沉淀在一定的条件下可以溶解在氨水中,有关反应的化学方程式为:Cu(OH)2+4NH3·H2O [Cu(NH3)4]2++2OH-+4H2O,有下列实验操作:
[Cu(NH3)4]2++2OH-+4H2O,有下列实验操作:
(1)操作1:在盛有3 mL 0.1 mol·L-1 CuSO4溶液的试管中滴加3 mL 0.2 mol·L-1 NaOH溶液,结果出现蓝色的悬浊液,有关反应的离子方程式为___________。
(2)操作2:在盛有3 mL 0.1 mol·L-1 CuSO4溶液的试管中滴加3 mL 0.2 mol·L-1氨水,结果也出现蓝色的悬浊液,有关反应的离子方程式为___________。
(3)在上述两种悬浊液中分别加入2 mol·L-1的氨水溶解,请从平衡移动的角度思考哪一种悬浊液更易溶解成为清液?__________(填“操作1”或“操作2”);理由是_____________。
(4)请你设计一个简单的实验方案验证上述观点(或理由)的可靠性。实验方案:______。
不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气。为了验证这一事实,某同学拟用下图装置进行实验(实验时压强为10l kPa,温度为0℃)。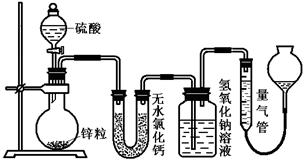
(1)若在烧瓶中放入1.30g锌粒,与c mol/L H2SO4反应,为保证实验结论的可靠,量气管的适宜规格是_____________ 。
A.200 mL B.400 mL C.500mL
(2)若1.30g锌粒完全溶解,测得盛氢氧化钠溶液的洗气瓶增重l.28 g ,则圆底烧瓶中发生反应的化学方程式为:_______________________________________。
(3)若烧瓶中投入a g锌且完全反应,氢氧化钠洗气瓶增重b g量气管中收集到VmL气体,则有方程:a g/65g·mol-1=b g/64g·mol-1+V mL / 22400 mL·mol-1,其依据的原理是____________________________。
(4)若在烧瓶中投入d g锌,再加入V L c mol/L 浓硫酸,充分反应后锌有剩余,测得盛氢氧化钠溶液的洗气瓶增重m g,则整个实验过程产生的混和气体中H2和SO2物质的量之比 n(H2)/n(SO2)=_______________(用含字母的代数式表示)。若撤走盛有无水氯化钙的U型管,n(H2)/n(SO2)的比值将(填
偏大、偏小或无影响)
正常人血液中葡萄糖(简称血糖)为3.61~ 6.11(单位:mmol·.L―1),测得某人血液中血糖的质量分数0.1%,已知葡萄糖的相对分子质量为180设血液密度为1g·cm―3,通过计算判定某人血糖指标是多少?某人血糖是否正常?