用NA表示阿伏加罗常数,下列叙述正确的是
| A.标准状况下,22.4LCCl4含有的分子数为NA |
| B.2.3gNa与足量的氧气发生反应,转移的电子数为0.2NA |
| C.通常情况下,32gO2与32gO3所含有的氧原子数均为2NA |
| D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-数目为NA |
下列实验中,由于错误操作导致所测出的数据偏低的是
| A.中和热(△H)的测定中,若使用简易装置时在大小烧杯之间没有垫碎泡沫塑料(或纸条) |
| B.用标准盐酸滴定氢氧化钠溶液,酸式滴定管洗净后,没有用标准盐酸润洗,所测出的碱液的浓度值 |
| C.食醋总酸含量测定实验中,用移液管移取食醋体积时视线俯视标准线移液 |
| D.在镀锌铁皮的锌镀层厚度的测定中,锌在酸中溶解后没有及时取出 |
下列有关离子浓度的比较正确的是的
A. 0.1mol·L—1氨水中,c(OH—)<c(NH4+)
B. 10mL 0.02mol·L—1HCl溶液与10mL 0.02mol·L—1Ba(OH)2溶液充分混合, c(Cl-)>c(Ba2+)>c(OH-)=c(H+)
C. 将0.1mol·L—1CH3COONa和0.1mol·L—1NH4Cl等体积混合后的溶液中,c(H+)+c(CH3COOH) >c(NH3·H2O)+c(OH—)
D. 0.1mol·L—1某二元弱酸碱性NaHA溶液中,c(H+) +c(H2A)=c(A2—)+c(OH—)
如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1 mol·L-1,工作一段时间后,测得导线中均通过0.01mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中不正确的是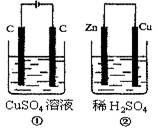
| A.右边电极上生成物质的物质的量:①=② |
| B.相同状态下电极上产生气体的体积:①=② |
| C.溶液的pH变化:①减小,②增大 |
| D.电极反应式①中阴极Cu2++2e-=Cu:②中负极:Zn-2e-=Zn2+ |
在恒容密闭容器中加入一定量的反应物后存在下列平衡:CO(g)+H2O(g)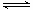 CO2(g)+H2(g)CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法不正确的是
CO2(g)+H2(g)CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法不正确的是
A.反应CO(g)+H2O(g)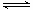 CO2(g)+H2(g)的 ΔH>0 CO2(g)+H2(g)的 ΔH>0 |
| B.在T2时,若反应处于状态D,则一定有ν正<ν逆 |
| C.平衡状态A与C相比,平衡状态A的c(CO)小 |
| D.若T1、T2时的平衡常数分别为K1、K2,则K1<K2 |
下列表示物质变化的化学用语正确的是
| A.已知在298K时下述反应的有关数据: C(s) + 1/2 O2(g) =" CO(g)" △H1 =-110.5 kJ·mol-1 C(s) + O2(g) = CO2(g) △H2=-393.5 kJ·mol-1, 则C(s)+CO2(g)="=" 2CO(g)△H=-172.5 kJ·mol-1 |
| B.KI溶液中滴加过量氯水发生反应的离子方程式为3Cl2+I-+3H2O ====6H++IO3-+6Cl- |
| C.等物质的量的NH4HCO3与Ba(OH)2溶液混合反应的离子方程式为Ba2++HCO3-+OH-=BaCO3↓+H2O |
D.用铜作电极电解硫酸溶液: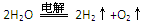 |