已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液形成无色溶液,其化学方程式是PbSO4+2CH3COONH4=Pb(CH3COO)2+(NH4)2SO4。当在醋酸铅溶液中通入H2S时,有黑色沉淀PbS生成,表示这个反应的有关离子方程式正确的是( )
| A.Pb(CH3COO)2+H2S=PbS↓+2CH3COOH |
| B.Pb2++H2S=PbS↓+2H+ |
| C.Pb2++2CH3COO-+H2S=PbS↓+2CH3COOH |
| D.Pb2++2CH3COO-+2H++S2-=PbS↓+2CH3COOH |
将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上并压紧(如下图所示)。在每次实验时,记录电压表指针的移动方向和电压表的读数如下表:(已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大。)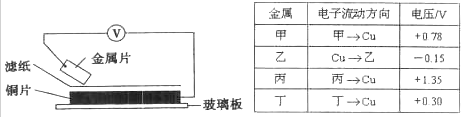
依据记录数据判断,下列结论中正确的是
| A.将甲、乙形成的合金露置在空气中,甲先被腐蚀 |
| B.金属乙能从硫酸铜溶液中置换出铜 |
| C.在四种金属中丙的还原性最弱 |
| D.甲、丁若形成原电池时,甲为正极 |
某研究性学习小组进行电化学实验,研究装置如图所示。
有关说法不正确的是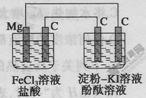
| A.镁为负极 |
| B.原电池中碳极的电极反应式为Fe3++e-=Fe2+ |
| C.电解池中阳极处先变红 |
| D.电解池中阴极的电极反应式为2H++2e-=H2↑ |
关于下列各图的叙述,正确的是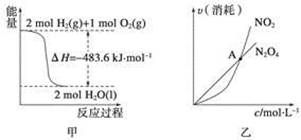

A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6 kJ/mol
B.乙表示恒温恒容条件下发生的可逆反应2NO2(g)  N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1 升温至t2
升温至t2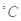 时,溶质的质量分数B>A
时,溶质的质量分数B>A
D.丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液
氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25 时:
时:
在20Ml0.lmol/L的氢氟酸中滴加0.lmol/L的NaOH V mL,下列说法正确的是
A.氢氟酸的电离方程式及热效应可表示为: |
B.当V="20" mL时,溶液中: |
C.当V="20" mL时,溶液中: |
D.当v>0时,溶液中一定存在 |
下列溶液中离子浓度大小关系错误的是
A.0.1 mol/L的NH4Cl溶液中: |
B.0.1mol/L的CH3COONa溶液中: |
C.0.1 mol/LNa2S的溶液中: |
D.pH=2的盐酸与pH=12的氨水等体积混合后: |