乳酸乙酯(2-羟基丙酸乙酯)常用于调制果香型、乳香型食用和酒用香精。为了在实验室制取乳酸乙酯,某研究性学习小组同学首先查阅资料,获得下列信息:
①部分物质的沸点:
| 物质 |
水 |
乙醇 |
乳酸 |
苯 |
乳酸乙酯 |
| 沸点/℃ |
100 |
78.4 |
122 |
80.10 |
154 |
②乳酸乙酯易溶于苯、乙醇;
③水、乙醇、苯的混合物在64.85℃时,能按一定的比例以共沸物的形式一起蒸发。该研究性学习小组同学拟采用如图所示(未画全)的主要装置制取乳酸乙酯,其主要实验步骤如下:
第一步:在三颈烧瓶中加入0.1mol无水乳酸、过量的65.0mL无水乙醇、一定量的苯、沸石……;装上油水分离器和冷凝管,缓慢加热回流至反应完全。
第二步:将三颈烧瓶中液体倒入盛有过量某试剂的烧杯中,搅拌并分出有机相后,再用水洗。
第三步:将无水CaCl2加入到水洗后的产品中,过滤、蒸馏。
(1)第一步操作中,还缺少的试剂是________;加入苯的目的是________;实验过程中,酯化反应进行完全的标志是____________。
(2)第二步中证明“水洗”已经完成的实验方案是__________。
(3)利用核磁共振氢谱可以鉴定制备的产物是否为乳酸乙酯,乳酸乙酯分子核磁共振氢谱中有____________个峰。
实验室制取乙烯的装置如下图所示,请回答: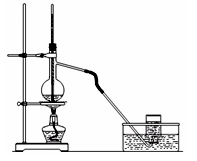
(1)反应中浓硫酸起剂和剂的作用;
(2)烧瓶内放碎瓷片的作用是;
(3)制取乙烯的化学方程式是: _。
(4)可能生成的主要有机副产物是;生成它的化学方程式为:。
Fe是人体不可缺少的微量元素,摄入含铁化合物可补充铁。硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下: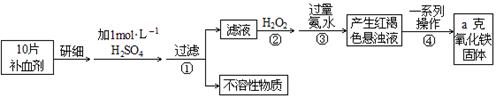
(1)步骤②加入过量H2O2的目的:;
(2)步骤③中反应的离子方程式:;
(3)步骤④中一系列处理的操作步骤:、洗涤、、冷却、称量。
(4)实验中用浓硫酸配制1 mol/L的稀硫酸,配制时用到的定量玻璃仪器有、。
(5)若实验无损耗,则每片补血剂含铁元素的质量g(用含a的代数式表示)。
瑞典化学家舍勒在研究软锰矿(主要成分是 )的过程中,将它与浓盐酸混合加热,产生了一种黄绿色、刺激性气味的气体——氯气。某学生使用这一原理设计如图所示的实验装置,并且利用制得的氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色、刺激性气味的气体——氯气。某学生使用这一原理设计如图所示的实验装置,并且利用制得的氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题: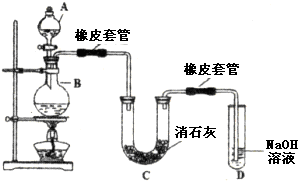
(1)B中发生反应的化学方程式是__________。
(2)漂白粉将在U形管中产生,其化学方程式是____________________。
(3)此实验结果所得 产率太低,经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
产率太低,经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成 ,为避免此副反应的发生,可采取的措施是______________________________。
,为避免此副反应的发生,可采取的措施是______________________________。
②试判断另一个副反应(写出此反应方程式):____________________。为避免此副反应发生,应采取的措施是______________________________。
(4)漂粉精同盐酸作用产生氯气: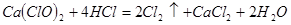 ,该反应中每生成
,该反应中每生成 ,转移电子的物质的量为__________
,转移电子的物质的量为__________ ,被氧化的
,被氧化的 的物质的量为__________
的物质的量为__________ 。
。
在室温下,化学反应I–(aq) + OCl–(aq) =OI–(aq) + Cl–(aq)的反应物初始浓度、溶液中的氢氧根离子初始浓度及初始速率间的关系如下表所示:
| 实验编号 |
I–的初始浓度 (mol·L-1) |
OCl–的初始浓度 (mol·L-1) |
OH–的初始浓度 (mol·L-1) |
初始速率v (mol·L-1· s-1) |
| 1 |
2 × 10–3 |
1.5 × 10–3 |
1.00 |
1.8 × 10–4 |
| 2 |
a |
1.5 × 10–3 |
1.00 |
3.6 × 10–4 |
| 3 |
2 × 10–3 |
3 × 10–3 |
2.00 |
1.8 × 10–4 |
| 4 |
4 × 10–3 |
3 × 10–3 |
1.00 |
7.2 × 10–4 |
已知表中初始反应速率与有关离子浓度关系可以表示为v=" k" [I–]1 [OCl–]b [OH–]c(温度一定时,k为常数)
①为了实施实验1,某同学取5mL0.02mol·L-1碘化钾溶液、5mL0.015 mol·L-1次氯酸钠溶液、40mL某浓度氢氧化钠溶液混合反应。则该氢氧化钠溶液物质的量浓度为 ________________
②实验2中,a=
③设计实验2和实验4的目的是;
④计算b、c值:b=;c=
⑤若实验编号4的其它浓度不变,仅将溶液的酸碱值变更为pH = 13,反应的初始速率v=。
某化学实验小组拟用以下装置由乙醇与浓硫酸共热制备乙烯,且进行乙烯的催化氧化实验。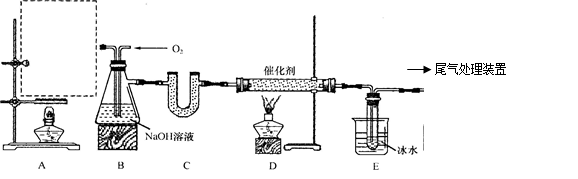
(1)在A处虚线框内绘出该实验装置图。
(2)制取乙烯的化学方程式为。
(3)装置B中盛有NaOH溶液,除了便于观察乙烯和氧气的流速以外,还具有的作用是:
①;②。
(4)若E中收集到的物质为CH3CHO,则D中发生反应的化学方程式为。
(5)用乙醇、浓硫酸共热制乙烯,所得乙烯产率较低,原因可能是(填字母序号)。
A.乙醇部分挥发 B.乙醇部分生成乙醚
C.乙醇被氧化为C、CO、CO2D.乙醇消去成乙炔