一定条件下,碳钢腐蚀与溶液pH的关系如下表。下列说法不正确的是( )
| pH |
2 |
4 |
6 |
6.5 |
8 |
13.5 |
14 |
| 腐蚀快慢 |
较快 |
慢 |
较快 |
||||
| 主要产物 |
Fe2+ |
Fe3O4 |
Fe2O3 |
FeO2- |
A.当溶液pH<4,碳钢主要发生析氢腐蚀
B.当溶液pH>13.5,碳钢腐蚀的正极反应式为O2+4H++4e-=2H2O
C.当溶液pH>6,碳钢主要发生吸氧腐蚀
D.煮沸除去氧气的碱性溶液中,碳钢腐蚀速率会减缓
对可逆反应4NH3(g)+ 5O2(g) 4NO(g)+ 6H2O(g),△H <0下列叙述正确的是()
4NO(g)+ 6H2O(g),△H <0下列叙述正确的是()
| A.化学反应速率关系是:2υ正(NH3)= 3υ正(H2O) |
| B.若升高温度,逆向反应速率增加,正向反应速率减小 |
| C.达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大 |
| D.达到化学平衡时,4υ正(O2)= 5υ逆(NO) |
下列反应中生成物总能量高于反应物总能量的是()
| A.碳酸钙受热分解 | B.乙醇燃烧 |
| C.铝粉与氧化铁粉末反应 | D.氧化钙溶于水 |
未来新能源的特点是资源丰富,在使用时对环境无污染或很少污染,且有些可以再生。下列属于新能源的是()
①天然气②煤③核能④石油⑤太阳能⑥燃料电池⑦风能⑧氢能
| A.①②③④ | B.⑤⑥⑦⑧ | C.③④⑤⑥ | D.除①②外 |
实验室中需要配制500mL0.10mol/L的NaOH溶液,就该实验回答下列问题。
(1)用天平称量NaOH固体g。称量NaOH固体需注意以下两个问题:
①因为NaOH具有腐蚀性,所以称量时,需选择烧杯盛装NaOH固体;
②称量必须迅速,原因是。
(2)接下来完成此实验你还需要选择的仪器有玻璃棒、烧杯、
(3)若从你配制的溶液中取出10mL溶液加水稀释至20mL,则此时溶液的物质的量浓度为
(4)下列操作对所配制的溶液浓度没有影响的是
| A.称量时已观察到NaOH表面潮湿 |
| B.将烧杯中溶解后的溶液立即注入容量瓶,然后再添加蒸馏水至刻度线 |
| C.定容摇匀后,又用胶头滴管向容量瓶中滴加蒸馏水至刻度线 |
| D.配制溶液前用蒸馏水洗涤容量瓶,但未烘干 |
请按要求填写下列各空
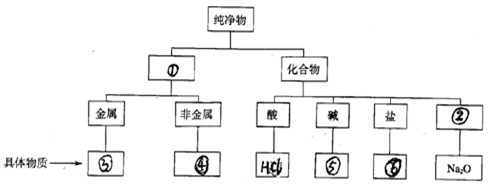
(1)完成下列树状分类图,并将HCl、Fe、H2、NaHCO3、Ba(OH)2五种物质填入分类图。
|
 溶液、
溶液、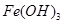 胶体、
胶体、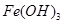 浊液三种分散系的特点,将空白处填写完整。
浊液三种分散系的特点,将空白处填写完整。
| 分散系 |
 溶液 溶液 |
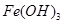 胶体 胶体 |
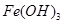 浊液 浊液 |
|
| 颜色 |
黄色 |
① |
红褐色 |
|
| 稳定性 |
稳定 |
② |
不稳定 |
|
| 光束照射现象 |
无一条光亮的通路 |
③ |
无一条光亮的通路 |
|
| 滤纸 |
滤后,滤液颜色 |
黄色 |
红褐色 |
④ |
| 半透膜 |
黄色 |
近无色 |
近无色 |