
(1)画出b元素的原子结构示意图 ,并写出元素b的单质在二氧化碳中燃烧的化学方程式: 。
(2)将a、b、c三种元素的最高价氧化物对应的水化物碱性由强到弱排序: (填写物质化学式)。
(3)写出元素c的氧化物与元素a的最高价氧化物对应的水化物反应的离子方程式: 。
(4)将e、f的最高价氧化物对应的水化物酸性较强的是: (填写物质化学式)。
(5)写出d元素的氢化物(一个分子共有三个原子)电子式: ,写出f元素与该氢化物反应的离子方程式: 。
(12分)盐酸、硫酸和硝酸是中学阶段所常见的“三大酸”。现请就三大酸与金属铜反应情况,填空回答下列问题:
(1)我们知道,稀盐酸不与Cu反应。在稀盐酸中加入H2O2后,则可使铜顺利溶解。该反应的化学方程式为。
(2)在一定体积的18mol/L的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积(填写“大于”、“等于”、或“小于”)lOOmL。
若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为。
(3)分别将等质量的铜片与等体积均过量的浓硝酸、稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出这可能是Cu2+浓度差异引起的,你同意这种看法吗?(填“同意”或“不同意”),原因是。另一同学提出溶液呈“绿色”是溶液中Cu2+与NO2共存的结果,请你设计实验探究此说法正确与否(简述实验方案和实验现象及由此得出的结论)
。
(12分)(1)在硫酸工业生产中,我国采用黄铁矿为原料生产SO2,反应的化学方程式为:,该反应在中进行。
(2)为了有利于SO2的转化为SO3,且能充分利用热能,采用了多层催化剂间有热交换器的接触室(见图)。按此密闭体系中气体的流向,则C处流出的气体为,A、B、C三处气体的温度由高到低的顺序为。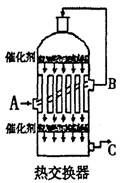
(3)在吸收塔中用吸收SO3,从吸收塔上部导出的气体再次通入,进行第二次氧化,再进行一次吸收后将尾气中很少的SO2净化回收,以防污染大气。
(4分)古希腊流传这样一个传奇故事:一批贩运纯碱的商船停泊在江边的沙岸部,商人们找不到石头来搭灶煮饭,就把船上的大块纯碱搬来,放在沙地上垫锅做饭,饭熟后商人们惊奇地发现“灶”变成了晶莹透明的固体。你认为这种固体可能是____________,其主要成分是________________________。
(8分)除去下列不纯物质中的少量杂质(括号内为杂质),请填入适当的试剂
(1)Fe(Al)____________(2)NH3(H2O)____________________-
(3)NO(NO2)____________ (4)NaCl溶液(Na2SO4)____________
有一质量为mg,相对分子质量为M的某种强碱M (OH)2,在一定温度下,完全溶解在水中得到VmL饱和溶液,若此溶液的密度为ρg/cm3,则该溶液中OH-的物质的量浓度为__________,溶质的质量分数为___________,此温度下该碱的溶解度为_________。