1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验中可以用图9所示装置制备1,2-二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。请填写下列空白:

(1)烧瓶a要求温度迅速升高到170℃发生反应,写出该反应的化学方程式 ;该反应类型为 。
(2)写出制备1,2-二溴乙烷的化学方程式 。
(3)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象 。
(4)容器c中NaOH溶液的作用是 ;e装置内NaOH溶液的作用是 。
(5)某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因(至少2点) 、 。
某同学帮助水质检测站配制480 mL 0.5 mol·L-1 NaOH溶液以备使用。
(1)该同学应选择________mL的容量瓶。
(2)其操作步骤如下图所示,
则如图操作应在下图中的________(填选项字母)之间。
A.②与③B.①与②C.④与⑤
(3)该同学应称取NaOH固体________g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小________(填字母),并在下图中选出能正确表示游码位置的选项________(填字母)。
附表 砝码规格
| a |
b |
c |
d |
e |
|
| 砝码大小/g |
100 |
50 |
20 |
10 |
5 |
(4)下列操作对所配溶液的浓度大小有何影响?
①转移完溶液后未洗涤玻璃棒和烧杯,浓度会________(填“偏大”、“偏小”或“无影响”,下同)
②容量瓶中原来有少量蒸馏水,浓度会________。
实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸和浓硝酸的混合酸加入反应器中。
②向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀。
③在50℃~60℃下发生反应。
④除去混合酸后,粗产品依次用蒸馏水和5%的NaOH溶液洗涤,最后用蒸馏水洗涤。
⑤将用无水氯化钙干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
(1)配制一定比例浓硝酸和浓硫酸混合酸时,操作注意事项是;
(2)步骤③的加热方式是;
(3)步骤④中,洗涤、分离粗硝基苯应使用的主要玻璃仪器是;
(4)步骤④中,粗产品用5%的NaOH溶液洗涤的目的是;
(5)纯硝基苯是无色、密度比水(填“大”或“小”)、具有气味的油状液体。
(10分)某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视________,直到因加入一滴盐酸后,溶液由黄色变为橙色,并____________为止。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是________(填字母序号)。
| A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸 |
| B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
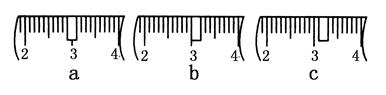
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为________mL。
(4)某学生根据3次实验分别记录有关数据如下表:
| 滴定次数 |
待测NaOH溶液的体积/mL |
0.100 0 mol·L-1盐酸的体积/mL |
||
| 滴定前刻度 |
滴定后刻度 |
溶液体积/mL |
||
| 第一次 |
25.00 |
0.00 |
26.11 |
26.11 |
| 第二次 |
25.00 |
1.56 |
30.30 |
28.74 |
| 第三次 |
25.00 |
0.22 |
26.31 |
26.09 |
依据上表数据列式计算该NaOH溶液的物质的量浓度。(保留4位有效数字)
(实验题)下图为配制250 mL 0.2 mol/L Na2CO3溶液的示意图。
回答下列问题:
(1)①中称得Na2CO3________g;选取容量瓶规格:______________
(2)容量瓶使用前检验漏水的方法是 ____________________。
(3)若出现如下情况,对所配溶液浓度有何影响?(填“偏高”“偏低”或“无影响”)
| A.某同学在第⑧步观察液面时俯视________; |
| B.没有进行操作步骤④和⑤________; |
| C.在第⑤步不慎有少量液体流到容量瓶外 ________。 |
| D.未经冷却趁热将溶液注入容量瓶中定容 ________。 |
E.摇匀后发现液面低于刻度线再加水 _______
某化学兴趣小组将两份等质量的硫粉分别在空气、氧气中燃烧,放出的热量是一样多还是不一样多?经过讨论、综合,根据观点分成了两组。
A组:在该过程中参加反应的硫与氧气量相等,反应物和生成物具有的能量都相等,故放出的热量相等。
B组:硫粉在氧气中燃烧比在空气中更剧烈,故在氧气中燃烧放出的热量多。
在老师的帮助下,他们决定用实验来探究其真相,在常温(25℃)下,实验过程如下(不考虑环境的影响):
①称取质量相等的两份硫粉;
②取一份硫粉放在燃烧匙中,伸入弹式量热计(剖面示意图如上)的密封器中;
③在密封器中充满空气的条件下,用电火花引燃,测出反应后内层中水的最高温度为t1;
④取另一份硫粉放在燃烧匙中,在密封器中充满氧气的条件下,用电火花引燃,测出反应后内层中水的最高温度为t2;
回答下列问题:
(1)若A组观点正确,则t1________t2(填“<”、“>”或“=”);
(2)根据实验所测数据显示:t1>t2,这说明结论与________(填“与A组观点”、“B组观点”或“都不”)符合;若填都不符合,那么哪种情况放出热量多?________________;
(3)请对t1>t2这一现象做出合理的解释:_________________________________________________;
(4)通过这个实验同时说明,当条件相同、反应物与生成物的量相同时,反应放出或吸收的热量多少与反应的剧烈程度________(填“有关”或“无关”)。