实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸和浓硝酸的混合酸加入反应器中。
②向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀。
③在50℃~60℃下发生反应。
④除去混合酸后,粗产品依次用蒸馏水和5%的NaOH溶液洗涤,最后用蒸馏水洗涤。
⑤将用无水氯化钙干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
(1)配制一定比例浓硝酸和浓硫酸混合酸时,操作注意事项是 ;
(2)步骤③的加热方式是 ;
(3)步骤④中,洗涤、分离粗硝基苯应使用的主要玻璃仪器是 ;
(4)步骤④中,粗产品用5%的NaOH溶液洗涤的目的是 ;
(5)纯硝基苯是无色、密度比水 (填“大”或“小”)、具有 气味的油状液体。
为验证氧化性Cl2 > Fe3+ > SO2,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验)。
实验过程:
I. 打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ. 打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ. 当B中溶液变黄时,停止加热,关闭K2。
Ⅳ. 打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ. 打开K3和活塞c,加入70%的硫酸,一段时间后关闭K3。
Ⅵ. 更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是。
(2)棉花中浸润的溶液为。
(3)A中发生反应的化学方程式。
(4)若将制取的SO2通入酸性高锰酸钾溶液可使溶液褪色,其离子方程式为。
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定能够证明氧化性Cl2 > Fe3+ > SO2的是(填“甲”“乙”“丙”)。
| 过程ⅣB溶液中含有的离子 |
过程ⅥB溶液中含有的离子 |
|
| 甲 |
有Fe3+无Fe2+ |
有SO42- |
| 乙 |
既有Fe3+又有Fe2+ |
有SO42- |
| 丙 |
有Fe3+无Fe2+ |
有Fe2+ |
某化学兴趣小组利用某废弃的氧化铜锌矿制取活性ZnO实验流程如下: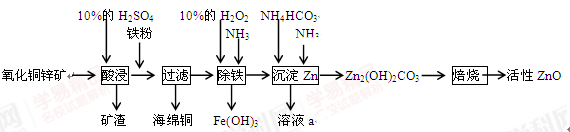
请回答下列问题:
(1)加入铁粉后发生反应的离子方程式为_________________________,________。
(2)甲、乙两同学选用下列仪器,采用不同的方法制取氨气。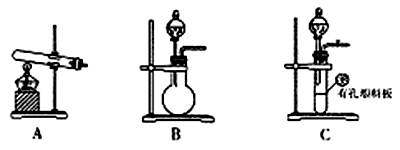
①甲同学使用的药品是熟石灰与氯化铵,则应选用装置_______(填写装置代号),生成氨气的化学方程式为_______________________________________;
②乙同学选用了装置B,则使用的两种药品的名称为_______________。
(3)H2O2的作用是____________________________________________________。
(4)除铁过程中得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能水处理剂(K2FeO4),该反应中氧化剂与还原剂的物质的量之比为____________。
(5)已知溶液a中含有CO2- 3、SO2- 4两种酸根阴离子,若只允许取用一次样品,检验这种离子存在的实验操作过程为_____________________________
(每空1分,共8分)实验室需要配制0.1 mol·L-1CuSO4溶液480 mL。
按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、______、________以及等质量的两片滤纸。
(2)计算,应选择下列正确________
| A.需要CuSO4 固体8g | B.需要CuSO4·5H2O晶体12.0 g |
| C.需要CuSO4·5H2O晶体12.5 g | D.需要CuSO4固体7.7 g |
(3)称量。所用砝码生锈则所配溶液的浓度会________(填“偏高”、“偏低”或“无影响”)。
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是_________________。
(5)转移、洗涤。在转移时应使用________引流,需要洗涤烧杯2~3次是为了______。
(6)定容,摇匀。
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶,贴好标签,注明配制的时间、溶液名称及浓度。
(8)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会________(填“偏高”、“偏低”或“无影响”)。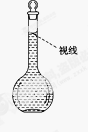
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。
请回答该实验中的问题。
(1)写出该反应的反应方程式:;并指明该氧化还原反应的还原剂是,氧化剂是。
(2)实验前必须对整套装置进行气密性检查,操作方法是。
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是。
(4)干燥管中盛装是的物质是,作用是。
(5)试管中收集气体是,如果要在A处玻璃管处点燃该气体,则必须对该气体进行,操作方法是
(12分)某化学小组为了证明SO2和Cl2的漂白性,设计了如图所示的实验装置: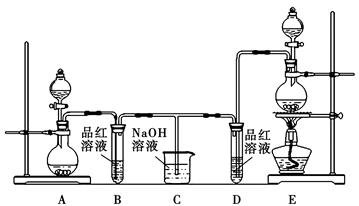
(1)他们制备Cl2依据的原理是:MnO2+4HCl(浓)  MnCl2+2H2O+Cl2↑,应选用上图A、E装置中的______________(填序号)制Cl2,反应中浓盐酸所表现出的性质是__________________。
MnCl2+2H2O+Cl2↑,应选用上图A、E装置中的______________(填序号)制Cl2,反应中浓盐酸所表现出的性质是__________________。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的液体加热,B试管中的现象是________________________________。
(3)NaOH溶液分别与两种气体反应的离子方程式是
______________________________________________________
________________________________________________。
(4)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。查阅资料得知:两种气体按体积比1∶1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是____________________________。