某化学兴趣小组为探究浓硫酸的性质,设计了如下图所示的装置进行实验。

(1)用“可抽动的铁丝”代替“直接投入铁片”的优点是 。
(2)说明SO2气体产生的实验现象是 ;装置C的作用是 。
(3)反应一段时间后,他们对试管A中溶液的金属离子进行探究,请完成相关试题:
①提出假设: 假设1:只含有Fe3+;
假设2:只含有Fe2+;
假设3:既有Fe2+,又有Fe3+。
②请设计实验方案验证假设3。
限选试剂:稀硫酸、KMnO4溶液、KSCN溶液、NaOH溶液、H2O2溶液。
| 实验步骤 |
预期现象 |
| 步骤一:用胶头滴管取出A试管中的溶液,用水稀释后,并分装在试管Ⅰ、Ⅱ中备用 |
 |
| 步骤二:检验Fe3+,往试管Ⅰ中, |
|
| 步骤三:检验Fe2+,往试管Ⅱ中, |
|
(4)已知C+2H2SO4(浓) 2SO2↑+CO2↑+2H2O,该反应体现浓硫酸的 性。
2SO2↑+CO2↑+2H2O,该反应体现浓硫酸的 性。
A.脱水性 B.强氧化性 C.吸水性
若要验证反应产物中同时混有SO2气体和CO2气体,可选择以下试剂进行实验:
①NaOH溶液②品红溶液③溴水④Ca(OH)2溶液,选择合适试剂并安排合理的顺序为 。
(15分)有机物M(分子式:C6H4S4)是隐形飞机上吸波材料的主要成分。某化学兴趣小组为验证其组成元素,并探究其分子结构进行了下列实验:
(1)验证组成元素
将少量样品放入燃烧管A中,通入足量O2,用电炉加热使其充分燃烧,并将燃烧产物依次通入余下装置。(夹持仪器的装置已略去)
①写出A中样品燃烧的化学方程式:________________________________________。
②装置B的目的是验证有机物中含氢元素,则B中盛装的试剂为________。
③D中盛放的试剂是________(填序号)。
a.NaOH溶液 b.品红溶液 c.酸性KMnO4溶液 d.溴的CCl4溶液 e.饱和石灰水
④能证明有机物含碳元素的现象是_________________________________________。
⑤装置Ⅰ、Ⅱ不能互换的理由是______________________________________________。
⑥燃烧管中放入CuO的作用是________________________________________________。
⑦指出装置F的错误:__________________________________________________。
(2)探究有机物M的分子结构高的对称性,氢原子的环境都相同。将2.04 g该有机物加入溴的CCl4溶液,充分振荡后溶液褪色,并消耗了0.03 mol Br2。
⑧该有机物分子结构中含有的官能团为________(填结构式)。
⑨有机物M的结构简式为________(填序号)。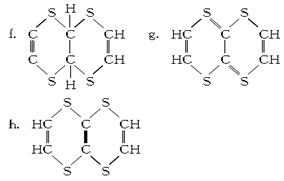
如图所示:在800 mL的大烧杯中放入碎纸屑,把盛有50 mL 0.50 mol·L-1盐酸的200 mL烧杯放到大烧杯中,两只烧杯间填满碎纸屑。用泡沫塑料板做成大烧杯盖,通过盖子插入一根玻璃搅拌器(末端呈半圆环的玻璃棒)和一只温度计,测定溶液的温度。迅速往盐酸溶液中加入50 mL 0.55 mol·L-1烧碱溶液,盖好,搅拌溶液,观察温度的变化。当温度保持稳定时,记录读数,取出装反应液的烧杯,倒出溶液,清洗干净,保持内外杯壁干燥。重复进行三次实验。用这一实验可以粗略测定中和热。
(1)烧杯间填满碎纸屑的作用是_____ 。
(2)要重复进行三次实验的目的是_____ 。
(3)烧杯如不盖硬纸板,求得的中和热数值将_____ (填“偏大”、“偏小”或“无影响”)。
(4)实验中若改用60 mL 0.50 mol·L-1盐酸和50 mL 0.55 mol·L-1烧碱溶液进行上述反应,与上述实验相比,所放出的热量_____ (填“相等”或“不相等”),所求中和热_____ (填“相等”或“不相等”),理由是_____。
(5)三次平行操作测得数据中,起始时盐酸与烧碱溶液温度相同,而终止温度与起始温度之差(t2-t1)分别为①2.3 ℃ ②2.4 ℃ ③2.9 ℃,则最终代入计算式的温度差的平均值为_____ ℃。
在一只小烧杯里,加入20 g Ba(OH)2·8H2O粉末,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后加入10 g NH4+Cl晶体,并用玻璃棒迅速搅拌。
(1)实验中玻璃棒的作用是_______。
(2)写出有关反应的化学方程式: _______ ,该反应属_______反应(填基本反应类型)。
(3)实验中观察到的现象有_______ 、 _______且反应混合物成糊状,反应混合物呈糊状的原因是_______ 。
(4)通过_______现象,说明该反应为_______热反应,这是由于反应物的总能量_______生成物的总能量。
(8分)经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
(1)定性分析:如图甲可通过观察___________________________________定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是____________________,
写出H2O2在二氧化锰作用下发生反应的化学方程式:
_____________________________________________________。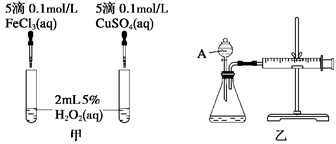
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为________,实验中需要测量的数据是_________________。
(12分)某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si元素非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。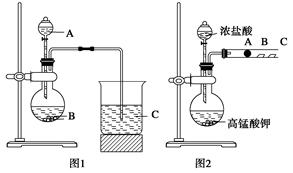
(1)甲同学设计实验的依据是_____________________________________________;
写出选用物质的名称:A____________,B__________,C____________;
反应的离子方程式为__________________________________________________________。
(2)乙同学的实验原理是__________________________________________;
写出B处的离子方程式: ___________________________________________________。