向盛有10滴0.1mol/L AgNO3溶液的试管中滴加0.1mol/L NaCl溶液,至不再有白色沉淀生成,再向其中滴加0.1mol/L KI溶液,观察到 ;然后向其中滴加0.1mol/L Na2S溶液,又观察到 。
用化学反应原理相关知识同答
I.根据下表所示化学反应与数据关系回答下列问题: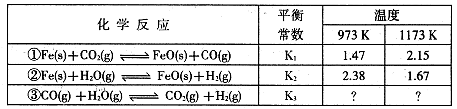
(1)反应①是(填“吸热"或“放热”)反应。
(2)根据反应①与②可推导出同温下K1、K2与K3之间的关系,则K3=(用K1、K2表示)。
(3)若反应③的逆反应速率与时间的关系如图所示: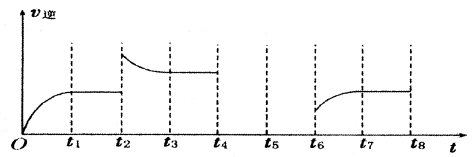
①反应在t1、t3、t7时都达到了平衡,若t2时只改变了一种外界条件j试判断:改变的条件可能是。
②若t4时降压,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系曲线。
II.请根据醋酸的电离平衡回答下列问题:
(1)常温下,0.1mol/L 的CH3COOH溶液中有l%的CH3COOH分子发生电离,则溶液的pH=。
(2)将上述溶液加蒸馏水稀释,在稀释过程中,下列各项中增大的是(填字母编号)。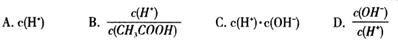
(3)25℃时,CH3COOH的电离平衡常数为1.75×10-5,现将一定量的CH3COOH与NaOH溶液混合,若测得混合液pH=5.6,则混合液中各离子浓度由大到小的顺序是。
有机物A是常用的食用油抗氧化剂,分子为C10H12O5,可发生如下变化:
已知B的相对分子质量为60,分子中只含一个甲基.C的结构可表示为:
(其中—x、一y均为官能团)。请回答下列问题:
(1)根据系统命名法,B的名称为;官能团一x的名称为;高聚物E的链节为;A的结构简式为。
(2)反应⑤的化学方程式为
(3)C有多种同分异构体,写出其中2种符合下列要求的同分异构体的结构简式、。
①含有苯环②能发生银镜反应③含有酚羟基
(4)从分子结构上看,A具有抗氧化作用的主要原因是 (填序号)。
A.含有苯环 B.含有羰基 C.含有酚羟基
随着世界粮食需求量的增加,农业对化学肥料的需求越越大。氮肥是需求最大的一种化肥。氮肥的生产和合理施用在农业生产中起着重大作用。合成氨及化肥生产流程示意图如下:
(1)目前,工业上用铁触媒作催化剂,在20~50 MPa、450℃左右用氮、氢混合气体在
中进行合成氨。则沿X方向回去的物质是。
(2)在侯氏制碱法中,从沉淀池中得到的母液要通人氨气、降温并加入(填化学式),目的是。
(3)沉淀池中的化学方程式是。
(4)工业上将氨催化氧化可制硝酸。在硝酸生产中,催化剂铂网在氨的催化氧化反应中起的作 用是。硝酸工业尾气对环境污染严重,若在催化剂存在下用甲烷将其中的一氧化氮还原为对空气无污染的物质,其反应的化学方程式为。
高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)△H= -28.5 kJ·(mol-1
2Fe(s)+3CO2(g)△H= -28.5 kJ·(mol-1
(1)已知:C(石墨)+CO2(g) 2CO(g)△H=" +" 172.5 kJ·mol-1
2CO(g)△H=" +" 172.5 kJ·mol-1
则反应:Fe2O3(S) +3C(石墨) 2Fe(s)+3CO(g)△H=kJ·mol-1
2Fe(s)+3CO(g)△H=kJ·mol-1
(2)冶炼铁反应 Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) △H=-28.5 kJ·mol-1的平衡常数表达式K= ,温度降低后,K值.(填“增大”、“不变”或“减小”)。
2Fe(s)+3CO2(g) △H=-28.5 kJ·mol-1的平衡常数表达式K= ,温度降低后,K值.(填“增大”、“不变”或“减小”)。
(3)在ToC时,该反应的平衡常数K=27,在1L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡.
| Fe2 O3 |
CO |
Fe |
CO2 |
|
| 甲容器 |
1.0 mol |
1.0 mol |
1.0 mol |
1.0 mol |
| 乙容器 |
1.0 mol |
2.0 mol |
1.0 mol |
1.0 mol |
①甲容器中CO的平衡转化率为
②下列说法正确的是(填字母)。
a.乙容器中CO的平衡转化率小于甲容器
b.甲、乙容器中,CO2的平衡浓度之比为2:3
c.当容器内气体压强保持不变时,标志反应达到平衡状态
d.当容器中气体密度保持不变时,标志反应达到平衡状态
(4)钢铁工业是国家工业的基础,请回答钢铁腐蚀与防护过程中的有关问题。
①下列哪个装置可防止铁棒被腐蚀(填编号)。
②在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图:A电极对应的金属是(写元素名称),B电极的电极反应式是。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因。
信息一:铬同镍、钴、铁等金属可以构成高温合金、电热合金、精密合金等,用于航空、宇航、电器及仪表等工业部门。
信息二:氯化铬酰(CrO2Cl2)是铬的一种化合物,常温下该化合物是暗红色液体,熔点为﹣96.5℃,沸点为117℃,能和丙酮(CH3COCH3)、四氯化碳、CS2等有机溶剂互溶。
(1)写出Fe(26号元素)原子的基态电子排布式为 。
(2)CH3COCH3分子中含有个π键,含有个δ键。
(3)固态氯化铬酰属于晶体,丙酮中碳原子的杂化方式为,二硫化碳属于(填极性”或“非极性”)分子。
(4)K[Cr(C2O4)2(H2O)2]也是铬的一种化合物,该化合物属于离子化合物,其中除含离子键、共价键外,还含有有键。
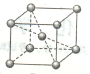
(5)金属铬的晶胞如下图所示,一个晶胞中含有个铬原子。