H2S是一种无色、有臭鸡蛋气味、有毒的可燃性气体,高温下可以分解,其水溶液叫氢硫酸(二元弱酸,较强还原性)。
(1)用30% FeCl3溶液作吸收液能吸收H2S气体,反应方程式为:2FeCl3+H2S=S↓+2FeCl2+2HCl,废吸收液经电解可循环使用。
①该反应中H2S显 (填字母代号)。
a、不稳定性 b、弱酸性 c、氧化性 d、还原性
②检验废吸收液中是否含有Fe3+的适宜试剂是 ;反应的离子方程式是 。
③强酸性的废吸收液电解可生成FeCl3和一种分子量最小的气体,则该反应的化学方程式是 。
(2)已知:H2S在高温下分解生成硫蒸气和H2。现测得某温度下,H2S分解过程中各物质的物质的量随时间变化关系如右图所示。

①表示H2的曲线是 (填“A”、“B”或“C”)。
②生成硫蒸气的分子式为 。
请根据官能团的不同对下列有机物进行分类。

(1)芳香烃:;(2)卤代烃:;
(3)醇:;(4)酚:;
(5)醛:;(6)酮:;
(7)羧酸:;(8)酯:。
医院抢救重金属中毒的病人时会采取哪些措施?常用的消毒方法有哪些?
(1),。
(2)有关葡萄糖反应的特征现象表现为:
与新制Cu(OH)2反应:。
与银氨溶液反应:。
(3)含碳原子数少于或等于10的烷烃中,其一氯代物只有一种的烷烃共有____种。
X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y、E的元素符号依次为、_______、 ____ ;
(2)XZ2与YZ2分子的立体结构分别是和,
相同条件下两者在水中的溶解度较大的是
(写分子式),理由是;
(3)Q的元素符号是,它属于第周期,
它的核外电子排布式为,在形成化合物时,它的最高化合价为.
某离子晶体晶胞如图所示,阳离子 X(●)位于立方体的顶点,阴离子Y(○)位于立方体的中心,试分析: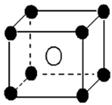
(1)晶体中Y的配位数是; X的配位数是;该晶体的化学式为 。
(2)晶体中在每个X周围与它最接近且距离相等的X共有个。
(3)该晶体的摩尔质量为M g/mol,晶体密度为ρ g/cm3,阿伏加德罗常数为NA,则晶体中两个距离最近的X中心间的距离为 cm。
按要求写出下列化学用语
(1) NaOH的电子式
(2)S原子核外电子排布式
(3)O原子的电子排布图
(4)Cl―离子的结构示意图