金可溶于王水(浓硝酸与浓盐酸的混合物):Au+HNO3+4HCl=HAuCl4+NO+2H2O,关于上述反应的有关说法错误的是
| A.盐酸作氧化剂 | B.HNO3被还原 |
| C.王水有很强的氧化性 | D.HAuCl4中Au的化合价为+3价 |
氧化还原反应实际上包含氧化和还原两个过程.(1)向氯酸钠的酸性水溶液中通入二氧化硫,该反应中氧化过程的反应式为:SO2 + 2H2O – 2e- → SO42- + 4H+;(2)向亚氯酸钠(NaClO2)固体中通入用空气稀释的氯气,该反应中还原过程的反应式为:Cl2 + 2e- → 2Cl-.在(1)和(2)反应中均会生成产物X,则X的化学式为
| A.NaClO | B.ClO2 | C.HClO | D.NaClO4 |
已知单位体积的稀溶液中,溶质的分子数或离子数越多,该溶液的凝固点就越低.则下列溶液凝固点最低的是
| A.0.02mol/L的蔗糖溶液 | B.0.01mol/L的硫酸银溶液 |
| C.0.01mol/L的氯化铝溶液 | D.0.02mol/L的氨水溶液 |
肉桂醛是一种实用香精,它广泛用于牙膏、洗涤剂、糖果以及调味品中.工业上可通过下列反应制备: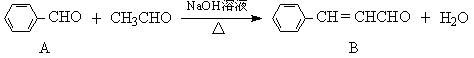
下列相关叙述正确的是
①B的相对分子质量比A大28;②A、B可用酸性高锰酸钾溶液鉴别;③B中含有的含氧官能团是醛基、碳碳双键;④A、B都能发生加成反应、还原反应;⑤A能发生银镜反应;⑥B的同类同分异构体(含苯环、包括B)共有5种;⑦A中所有原子一定处于同一平面
A.只有①②⑤B.只有③④⑤C.只有④⑤⑥D.只有②⑤⑥⑦
某温度下,在一密闭容器中发生如下可逆反应:2E(g)  F(g)+xG(g);△H<0。若起始时E浓度为a mol·L-1,F、G浓度均为0,达平衡时E浓度为0.5a mol·L-1;若E的起始浓度改为 2a mol·L-1,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是
F(g)+xG(g);△H<0。若起始时E浓度为a mol·L-1,F、G浓度均为0,达平衡时E浓度为0.5a mol·L-1;若E的起始浓度改为 2a mol·L-1,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是
| A.升高温度时,正反应速率加快、逆反应速率减慢 |
| B.若x=l,容器体积保持不变,新平衡下E的体积分数为50% |
| C.若x=2,容器体积保持不变,新平衡下F的平衡浓度大于0.5a mol·L-1 |
| D.若x=2,容器压强保持不变,新平衡下E的物质的量为a mol |
下列溶液中微粒的物质的量浓度关系一定正确的是
| A.25℃时pH=10的NaOH溶液与pH=10的氨水中:c(Na+)>c(NH4+) |
| B.物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合: c(CH3COO-) +2c(OH-) = 2c(H+) + c(CH3COOH) |
| C.在NaHA溶液中(H2A为弱酸):c(Na+)>c(HA-)>c(OH-)>c(H+) |
| D.室温下,向0.01 mol·L-1 NH4HSO4溶液中滴加NaOH溶液至中性: |
c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)