常温下,0.2 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合后(忽略混合前后溶液体积的变化),溶液的pH<7,则下列有关此溶液的叙述正确的是( )
| A.溶液中由水电离产生的H+浓度为1×10-7 mol/L |
| B.c(CH3COO-)+c(CH3COOH)-c(Na+)=0.05 mol/L |
| C.溶液中CH3COOH的电离程度小于CH3COONa的水解程度 |
| D.溶液中离子浓度的大小关系为:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
锗酸铋(简称BGO)是我国研制成功的一种性能优良的闪烁晶体材料,其中Ge元素处于最高价态,铋元素的价态与它跟氯形成某些共价化合物所呈的价态相同,且此氯化物中铋具有8电子稳定结构,可表示为[BixGeyOz]n。则式中x等于()
| A.2z-4y |
B.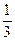 (2z-4y) (2z-4y) |
C.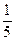 (2z-4y) (2z-4y) |
D.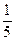 (2z-3y) (2z-3y) |
三氯化氮分子中每个原子其最外层均达到8电子稳定结构,下列关于三氯化氮的叙述正确的是()
A.NCl3的电子式应表示为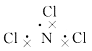 |
| B.在NCl3分子中N为+3价,跟水发生水解反应的产物是HNO2和HCl |
| C.NCl3跟水反应的产物为HClO和NH3 |
| D.NCl3跟水反应生成NH4Cl、O2和Cl2 |
在一定条件下,PbO2与Cr3+反应,产物是 和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为()
和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为()
| A.3.0 mol |
| B.1.5 mol |
| C.1.0 mol |
| D.0.75 mol |
向100 mL 12 mol·L-1的浓HNO3中加入足量的Cu片,充分反应后,被还原的HNO3的物质的量()
| A.等于0.3 mol |
| B.等于0.6 mol |
| C.小于0.6 mol |
| D.介于0.3 mol和0.6 mol之间 |
工业上以NH3为原料制HNO3,将m g NH3完全转化为HNO3,且将生成的HNO3全部溶解于反应生成的水中,此硝酸溶液的质量分数为()
| A.77.8% |
| B.50% |
| C.63.5% |
| D.98% |