某化学兴趣小组在做氢氧化钠溶液和稀硫酸中和反应的实验时,忘记滴加指示剂而无法判断酸碱是否恰好完全反应,于是,对反应后溶液中的溶质进行探究。
【提出问题】该溶液中的溶质是什么?
【查阅资料】Na 2SO 4溶液的pH=7
【猜想与假设】
猜想Ⅰ溶液中的溶质只有Na 2SO 4
猜想Ⅱ溶液中的溶质是Na 2SO 4和H 2SO 4
猜想Ⅲ溶液中的溶质是
【进行实验】
实验操作 |
实验现象 |
实验结论 |
①取少量反应后的溶液于 试管中,滴入酚酞溶液 |
未见变红 |
猜想Ⅲ错误 |
②再取少量反应后的溶液于 另一支试管中,向其中加入Na 2CO 3溶液 |
|
猜想Ⅱ正确 |
实验②中反应的化学方程式是 。
【反思拓展】若想验证猜想Ⅱ正确,在实验②中还可以用以下 代替Na 2CO 3溶液。
A.Zn B.Cu C.CuO D.BaCl 2溶液
【交流提升】在探究该中和反应的产物组成时,只需一步就可达到目的:取反应后溶液少许于试管中,滴加 溶液观察现象即可。
骗子往往披着科学的外衣,而科学可以给我们一双明辨是非的眼睛。例如:有人提出使用“高科技的添加剂”可以使水变成汽油。小明同学在学习过物质构成的奥秘后,认为可以用物质组成的观点解开这个骗局。
提出问题:根据水的组成和汽油的组成判断,水是否可以变成汽油。
猜想与验证:
(1)确定水的组成.实验装置示意图如下: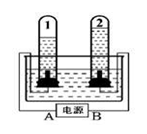
图“2”中收集的气体能 ,电解水的符号表达式是 。
实验结论:水是由氢元素和氧元素组成的。
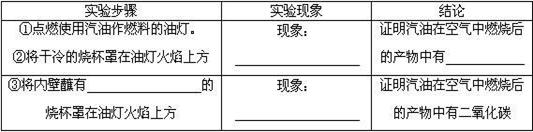
(2)确定汽油的成分.操作如下:
|
小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题。
她设计并完成了下表所示的探究实验:
| 实验操作 |
实验现象 |
实验结论或总结 |
||
| 结论 |
总结 |
|||
| 实验一 |
取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 |
有气泡产生,木条不复燃 |
过氧化氢分解产生氧气,但是。 |
二氧化锰是过氧化氢分解的催化剂 |
| 实验二 |
向盛水的试管中加入二氧化锰,伸入带火星的木条 |
没有明显现象 |
||
| 实验三 |
二氧化锰能加快过氧化氢的分解,反应文字表达式为: 。 |
(1)请你帮小丽同学填写上表中未填完的空格。
(2)在小丽的探究实验中,“实验一”和“实验二”起的作用是 。
(3)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明。
第一方面的实验操作中包含了两次称量其目的是:;
第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验。其目的是 。
现有失去标签的两瓶无色溶液:氢氧化钠溶液和稀盐酸。某化学探究小组打算用化学方法加以区别。请回答:
在不选用酸碱指示剂、pH试纸的情况下,按表中方法一(示例)填写。所选试剂须属于不同物质类别(单质、氧化物、酸、碱、盐、有机物等)。
| 所选试剂 |
判别方法 |
|
| 方法一 |
锌 |
取少量样品分别与锌反应,有气体产生的是稀盐酸,没有的是氢氧化钠溶液。 |
| 方法二 |
||
| 方法三 |
期末化学实验老师整理药品时,拿出一瓶久置的氢氧化钙粉末[Ca(OH)2)],他让小王和大伟对这瓶氢氧化钙粉末的组成进行实验探究。
(1)提出问题:这瓶氢氧化钙是否已经生成碳酸钙(CaCO3)而变质?
(2)进行猜想:
①氢氧化钙全部变为碳酸钙;②氢氧化钙部分变为碳酸钙;③氢氧化钙没有变质。
(3)设计实验方案、进行实验:下表是对猜想①进行实验探究的过程示例:
| 实验步骤 |
实验现象 |
实验结论 |
| 取样,加适量水,搅拌,过滤 ①取少量滤液于试管中,滴入酚酞试液 ②取少量滤渣于试管中,加入盐酸 |
①滤液不变色 ②有气泡产生 |
氢氧化钙全部变 为碳酸钙 |
请你另选择一种猜想参与探究,完成下表。
| 实验步骤 |
实验现象 |
实验结论 |
| 取样,加适量水广搅拌,过滤 ①取少量滤液于试管中,滴入酚酞试液 ②取少量滤渣于试管中,加入盐酸 |
① |
|
| ② |
(4)反思与应用:
氢氧化钙变质是由于与空气中的_________________发生反应的缘故,反应的化学程式是:___________________________________,因此氢氧化钙应______保存。
炎炎夏日,喝上一杯汽水会给我们带来清爽凉快的感觉。如图是某种雪碧汽水标签中的部分内容,小明同学通过查阅资料得知:柠檬酸是一种无色晶体,能溶于水,属于有机酸,具有酸的通性。香料、苯甲酸钠、白砂糖等不显酸性。
(1)以上信息中属于柠檬酸物理性质的是。
(2)小明想利用此种雪碧汽水和同学们进一步验证柠檬酸的酸性:
①小明首先将适量的雪碧汽水倒入一洁净的试管中,然后滴加紫色石蕊试液,发现石蕊试液变红色。据此,小明断定柠檬酸确实具有酸性。他做出这种判断的依据是 。
②小红认为小明的实验结论不够严密,她的理由是;她建议在原来实验的基础上再进行一步操作,即把①中已经变红的混合液体加热,若看到 ,这样就能充分证明柠檬酸确实具有酸性了。