某氯化钡样品23.1g中含有少量的氯化钠,某同学进行了如图所示的实验.请计算:
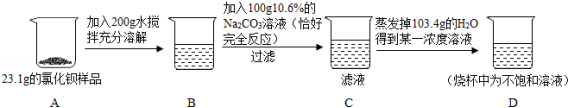
(1)过滤后得到沉淀多少克?
(2)原样品中氯化钡的质量分数?(计算结果精确到0.1%)
(3)求D烧杯中所得溶液的溶质质量分数是多少?
现有含杂质的氯化镁样品10
(杂质不溶于水,也不参加反应),向其中加入一定量的氢氧化钠溶液恰好完全反应,过滤,得到117
质量分数为10%的溶液.求:
(1)样品中氯化镁的质量分数;
(2)所加入氢氧化钠溶液的质量分数(计算结果精确到0.1%).
人体摄入锌不足会引起多种疾病,缺锌者可在医生指导下通过服用葡萄糖酸锌口服液来补锌.已知葡萄糖酸锌的化学式为
.填空:
(1)葡萄糖酸锌中属于微量元素的是;
(2)葡萄糖酸锌的相对分子质量为;
(3)葡萄糖酸锌中锌元素的质量分数为(计算结果精确到0.1%).
某兴趣小组用
镁条与溶质质量分数为
的稀硫酸反应.测得产生氢气的质量与稀硫酸的质量关系如图(假设镁条中除表面含有氧化镁外,没有其它杂质).
(1)当稀硫酸的质量为
,产生的氢气的质量为
.
(2)用化学方程式说明当稀硫酸的质量为
时,为什么不产生氢气
(3)计算镁条中镁元素的质量分数(写出计算过程).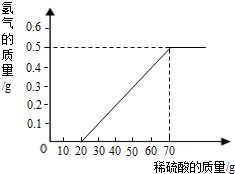
将20g含杂质(杂质不溶于水,也不溶于酸)的锌样品,与一定质量的稀硫酸恰好完全反应,所得溶液质量80.5g,同时生成氢气0.4g,试计算:
(1)样品中锌的质量为:g。
(2)完全反应后所得溶液中溶质的质量分数(写出计算过程)。
型禽流感是一种新型禽流感,于2013年3月底在上海和安徽两地率先发现,已经造成多人死亡,帕拉米韦是一种新型的抗流感病毒药物,属神经氨酸酶抑制剂,对抑制 禽流感有一定的效果,其化学式为: (其相对分子质量为328),回答以下问题:
(1)帕拉米韦是由种元素组成.
(2)帕拉米韦中H、N两种元素的质量比为:;
(3)帕拉米韦中碳元素的质量分数为:.