观察是学习化学的重要方法。我们可以运用自己的感官,也可以借助仪器通过实验,观察物质及其变化的条件、现象和结果。
观察与思考一:蜡烛在空气中燃烧

观察与思考二:在密闭容器内,蜡烛燃烧过程中O 2体积分数的测定
实验1:一定条件下,蜡烛在一瓶空气中燃烧。某同学利用O 2传感器,测定燃烧过程中O 2的体积分数。(如下图所示)

观察实验结果图,初始时O 2的体积分数是 %,蜡烛熄灭时O 2的体积分数是 %。
实验2:相同实验条件下,某同学另取一瓶混有空气的O 2进行测定(初始时O 2的体积分数是30%)。
结合已有信息,合理猜想:蜡烛熄灭时O 2的体积分数(与实验1相比较)。
请写出两种不同情况并分别说明理由。
【温馨提示:实验操作合理,蜡烛相同且量足够,忽略仪器误差】
猜想1及理由: ;
猜想2及理由: 。
同学们在帮助老师整理实验室时,从1、2号橱窗中发现了两瓶失去标签的黑色粉末药品,并确定了这两瓶黑色粉末是木炭粉、铁粉、氧化铜、高锰酸钾中的两种。他们继续进行了分析、试验和反思:
【查阅资料】CuO、Fe2O3等金属氧化物与酸反应,生成盐和水
(1)分析:小燕同学认为一定不是高锰酸钾,原因是_______________________;
(2)实验一:
| 实验操作 |
||
| ①取一种黑色粉末少许,加入到稀硫酸中 |
黑色粉末溶解,溶液颜色变_________ |
此粉末是氧化铜 |
| ②取另一种黑色粉末少许,加入到稀硫酸中 |
黑色粉末不溶解,没看到气体产生 |
此粉末一定不是铁粉 |
(3)反思:小华同学认为不做实验①,运用逻辑推理的方法也能得出其中之一是氧化铜的结论,原因是:__________________________________________________;
(4)实验二:他们又进行了如下实验:将两种黑色粉末混合加热(实验装置如下图),发现黑色粉末逐渐变_______,澄清石灰水变____________。写出两种黑色粉末发生反应的化学方程式__________________。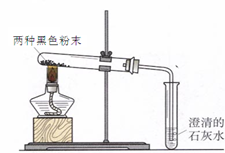
一男孩在排污井盖上燃放鞭炮,点燃了排污井内的气体,井盖被炸飞,男孩被井盖击伤.
【提出问题】排污井内气体的主要成分是什么?
【查阅资料】排污井内的有机物在一定的条件下发酵产生了气体,其成分可能含有CO、CO2、CH4等.
【提出猜想】某兴趣小组同学对排污井内气体含有上述气体中最少2种成分的猜想如下:
猜想Ⅰ:有CO2、CH4猜想Ⅱ:有CO、CH4
猜想Ⅲ:有CO、CO2猜想Ⅳ:有CO、CO2、CH4
【实验方案】小组同学共同设计了下图所示的装置并经行探究.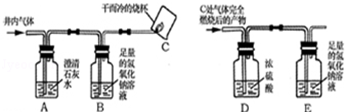
【问题讨论】
(1)装置A出现浑浊,证明猜想 不正确.
(2)小明通过装置C处 的现象,证明猜想Ⅲ不成立.小芳对此提出了疑义,小芳认为要
在 位置,再增加一个上图中 (填序号)装置,才能证明猜想Ⅲ不成立.
(3)为了进一步确认气体中是否含有一氧化碳,小明将装置C处气体完全燃烧后的产物依次通过装置D、E,经实验测定装置D增重1.8g,装置E增重2.2g,由此证明猜想 成立.
(4)小明认为要证明排污井内气体是否含有CO,可以不用装置B,小芳则认为需要使用装置B,你认为装置B的作用是 .
科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环(如图所示)。
某化学小组的同学对此非常感兴趣,在老师的指导下,设计如下装置探究上述设想的反应原理是否可行。
(1)能证明装置A“释放CO2”的现象是 ;
(2)装置B在实验结束撤掉酒精喷灯时的作用是 ;
(3)上述反应结束后,小组同学对D中固体的成分进行探究,以证明是否“捕捉”到CO2。
【猜想与假设】
D中的固体可能为:I.只有氧化钙;Ⅱ.氧化钙与碳酸钙;Ⅲ.只有碳酸钙
【进行实验】
①甲同学从D中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物。甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅲ成立。乙同学认为上述实验不足以证明猜想Ⅲ成立,其理由是 。
②乙同学从D中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生。乙同学据此认为试管中的固体只有氧化钙,即猜想I成立。丙同学认为乙的实验不足以证明猜想I成立,理由是 。
③丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想Ⅱ成立,请完成他的实验报告。
| 实验步骤 |
实验现象 |
实验结论 |
| 猜想Ⅱ成立 |
(4)通过以上探究,小组同学认为科学家的设想在反应原理上是可行的。该设想的优点有 (填字母序号)。
A.原料易得
B.充分利用太阳能
C.释放出的CO2可作为资源加以利用
实验是进行科学探究的重要方式,请填写下列空格: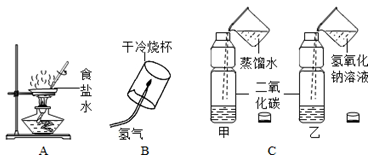
(1)在蒸发食盐水获取食盐晶体时(图A),应在蒸发皿内出现 时,即停止加热.
(2)在点燃氢气等可燃性气体前(图B),一定要先 .
(3)某同学取甲、乙两个完全相同的装满二氧化碳的塑料瓶(图C),向甲、乙两瓶中分别倒入相同体积的蒸馏水和氢氧化钠溶液,然后将两瓶迅速拧紧瓶盖,振荡,观察现象.该实验的探究目的是 .
(4)用坩埚坩夹持一团钢丝棉,在酒精灯火焰上灼烧至红热,未见钢丝棉燃烧,然后将钢丝棉迅速插入盛有氧气的集气瓶中,钢丝棉在氧气中剧烈燃烧.据此可分析得知,钢丝棉能否燃烧与 有关.
使用甲醇(CHOH)作为汽车的燃料,可以减少汽车尾气对环境造成的污染,某研究性学习小组为了探究甲醇在氧气中燃烧的产物,将甲醇在一定量的氧气中点燃,再将燃烧后的混合气体通过如下的装置进行实验,请填空:
(1)为尽可能多地检验出甲醇的燃烧产物,如图所示装置的正确连接顺序为:
混合气体→ → → →D(填写装置序号,装置不重复使用).
(2)该学习小组的同学通过正确的设计并进行实验,在实验过程中观察到的部分现象为:D和A中①装置内的澄清石灰水均变浑浊,而A中③装置内的澄清石灰水不变浑浊,根据实验结果并通过分析推理,得出这次实验中甲醇的燃烧产物为 (填写化学式).
(3)如果将A中②、③装置去掉,则可能会影响对燃烧产物中 的检验.