碱石灰是由CaO和NaOH固体组成的混合物,它是实验室常用的干燥剂。同学们在实验室里发现一瓶久置的碱石灰样品,为探究其成分,同学们对这包碱石灰样品展开了探究。
【查阅资料】BaCl2溶液显中性。
【提出猜想】该碱石灰样品的主要成分可能含有CaO、NaOH、CaCO3、Na2CO3和 。
【实验探究】
步骤Ⅰ:取部分该碱石灰样品于小烧杯中,加少量水后无放热现象,再继续加足量水,搅拌、静置后有白色沉淀产生。
步骤Ⅱ:取步骤Ⅰ小烧杯内的上层清液少量于试管中,滴加过量BaCl2溶液,有白色沉淀产生。
步骤Ⅲ:将步骤Ⅱ所得物质过滤,向滤液中滴加酚酞溶液,溶液变红色。
【解释与结论】
(1)该碱石灰样品中一定含有的物质是 ,一定不含有的物质是 。
(2)写出步骤Ⅱ中生成白色沉淀的化学方程式: 。
(3)步骤Ⅲ所得溶液中除酚酞外还含有的溶质是 。
【迁移应用】写出不能用碱石灰干燥的两种气体的化学式: 。
蕲春实验中学化学课外活动小组选择如下相应的装置对某有机物燃烧产物进行探究,并对该有机物成分进行测定: A B C D E
A B C D E
[提出假设]根据质量守恒定律,可得出该有机物燃烧产物可能为①CO2、H2O;②H2O、CO;③CO2、H2O、CO。
[设计实验]
(1)余成林同学选择D、E分别验证假设①,如观察到E中现象,则证明有H2O,如观察到D中现象,则证明有CO2;
(2)翁京京同学选择装置A、C、D、E按照E D C A 的连接顺序一次性来验证假设②,实验时发现E中无水CuSO4变蓝,D中澄清石灰水变浑浊,A中黑色CuO变成光亮红色,则假设②是否成立,得出这个结论的理由是:。
(3)汪俊同学同样按照E D C A D的连接顺序来验证假设③,如该假设成立,则丙同学应应观察到____________________________________________现象,那么该实验装置还有何不足: _______________ 。
(4)现假设该有机物燃烧产物为CO2、H2O,有甲、乙两组同学选择B、C装置分别两种方法测定它的组成,得出两组数据(连接顺序与数据如下表)
| 有机物 的质量 |
装置的连接顺序 |
 装置的质量 装置的质量 实验前实验后 实验前实验后 |
|
| 甲组 |
1.6克 |
C接B |
B 200克 B 202.3克 C 200克 C 201.7克 |
| 乙组 |
1.6克 |
B接C |
B 200克 B 201.8克 C 200克 C 202.2克 |
你认为甲、乙两小组的两种方法哪种正确?,理由是: _____。请你选择、计算得出有机物各元素的质量比:。
某学校“我与化学”学习小组发现,铜绿 [Cu2 (OH)2CO3] 受热分解后,除生成CO2和水蒸气外,试管中还有一些黑色粉末状固体。于是他们就通过实验探究分析黑色固体的组成,并验证产生的气体。请你参与一起分析探讨:
(1) 试管中的黑色团体可能是炭粉,也可能是氧化铜,还可能是。
(2) 经查阅资料可知炭粉不能与酸反应,也不溶于酸,而氧化铜则可与酸反应而溶解。于是他们先向试管中的黑色固体里加入一种溶液来检验黑色固体究竟是什么?你认为他们可加的溶液是(填化学式)
(3) 具体分析如下:假如黑色固体是炭粉,应该看到的现象是;如果发现,该黑色固体则是氧化铜;假如现象为,才证明第三种可能成立。
(4) 若用右图装置验证两种气体生成物,
应将生成的混合气体先通过(填“A”或“B’’”)装置,不然就会有影响,原因是。当将气体通入装置A进行验证时,气流应从通入。
实验室有两瓶失去标签的试剂,其中一瓶是固体,另一瓶是液体。化学学习小组分别各取少量这两种试剂在试管中混合,发现立即产生一种无色气体。老师要求他们探究这两种试剂反应产生的气体究竟是什么?验证实验方案如下:
试根据你的猜想写出产生此气体的化学方程式。
如果要求你制取该气体,采用的发生装置可选取下图中的(填序号).
AB CDE
有同学提出此无色气体还有可能是另外一种气体,也请写出这种气体_______(填化学式)
做"镁带在空气中燃烧"实验时,小科同学发现生成物中有少量黑色固体.黑色固体是镁和什么物质反应所产生的?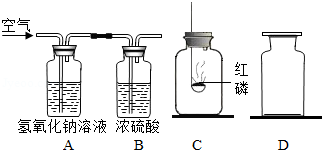
他提出下列猜想:
猜想一:黑色固体可能是镁和氮气反应的产物;
猜想二:黑色固体可能是镁和二氧化碳反应的产物.
为了验证上述两个猜想,小科设想:
(1)让空气通过
、
装置,其中A装置的作用是 ;
(2)用
瓶收集通过
、
装置后的气体,并加入足量的红磷燃烧;待
瓶冷却后,再把点燃的镁带放入
瓶中.
经过思考发现,由于收集气体时相关气体的密度差异及C瓶冷却后瓶内外的气压差异,达不到预期效果.
于是,他在老师的帮助下获得了这种气体,观察到镁带在该气体中燃烧并有淡黄色的固体产生;然后用
瓶收集一瓶气体,把点燃的镁带放入
瓶中,观察到镁带在
瓶也能燃烧,同时有白色和黑色固体生成.
通过以上实验,得出结论:猜想正确.同时,他对燃烧有了新的认识:
为检测某化工厂排放的废液中是否含有
,同学们设计了如下方案,并进行了实验.
| 方案 |
步骤 |
现象 |
结论 |
| Ⅰ |
①取样品.滴加
溶液 ②对步骤①反应后的混合物进行过滤,在滤渣中滴加稀盐酸 |
①有白色沉淀产生 ②无明显现象 |
废液中含有
|
| Ⅱ |
①取样品,滴加过量②在步骤①的溶液中滴加
溶液 |
①无明显现象 ②有白色沉淀产生 |
废液中含有
|
| Ⅲ |
①取样品,滴加
溶液 ②对步骤①产生的混合物进行过滤,在滤渣中滴加稀硝酸 |
①有白色沉淀产生 ②无明显现象 |
废液中含有
|
(1)方案Ⅱ的实验结论如果正确,步骤①中滴加的物质是.
(2)方案Ⅰ和Ⅲ中,结论不成立的方案是,理由是.
(3)方案Ⅲ的滤渣中,滴加稀硝酸是为了排除的干扰.