加热碳酸氢铵时闻到了刺激性气味,引起了同学们对氨气的兴趣,决定对其进行探究。
(一)探究性质与变化
【实验方案】如图所示

【实验现象】
(1)实验一中的现象是 。
(2)实验二中先滴入浓氨水,一段时间后,再滴入浓盐酸。滴入浓盐酸后观察到的现象是:①集气瓶中从下至上出现白烟,② (写一点)。
【实验结论】
(3)微观上,说明微粒具有的性质是 。宏观上,从物质的性质或变化的角度分析,你得出的结论是 (写一点)。
【反思与评价】
(4)实验二避免了实验一的不足,改进后的优点有 (写一点)。
(二)验证氨气中氮、氢两种元素的质量比
【查阅资料】
(5)氨气在加热条件下能与氧化铜反应:2NH3+3CuO 3X+N2+3H2O,X的化学式是 。
3X+N2+3H2O,X的化学式是 。
【设计方案】如图所示:(假定氮气被完全吸收)

【数据处理与误差分析】
充分反应后,测得A、B、C三个装置在反应前后的质量变化如下表所示
装置 |
A |
B |
C |
数据 |
减少了4.8g |
增加了6.0g |
增加了2.8g |
(6)甲同学利用A、B、C三组装置所提供的数据,乙同学利用B、C两组装置所提供的数据,计算出的氮、氢元素的质量比都与理论值明显不符,分析产生误差的原因是 。
(7)若用A、C两组装置所提供的数据计算,与理论值是否相符?写出简单的计算过程证明你的结论 。
(三)探究用途与制法
(8)在一定条件下,可用氮气和氢气制得氨气。工业上常用氨气生产氮肥(NH4)2SO4,施肥时,要避免与之混用的是 (填序号)。
A.硝酸钾 B.草木灰(主要成分是K2CO3)
C.熟石灰 D.氯化钾
(9)工业上生产的(NH4)2SO4中常常混有少量KCl,检验其是否含有KCl的操作方法是 。
附:部分碱、酸、盐的溶解性表(20℃)
阴离子/阳离子 |
OH﹣ |
NO3﹣ |
Cl﹣ |
SO42﹣ |
H+ |
溶、挥 |
溶、挥 |
溶 |
|
K+ |
溶 |
溶 |
溶 |
溶 |
NH4+ |
溶、挥 |
溶 |
溶 |
溶 |
Ba2+ |
溶 |
溶 |
溶 |
不 |
Ag+ |
﹣ |
溶 |
不 |
微 |
说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“﹣”表示那种物质不存在或遇到水就分解了。
实验室现有石灰石、稀盐酸、火柴、药匙、升降台、木条、棉花、镊子及以下仪器:

(1)若要制取二氧化碳,应选择的仪器有①锥形瓶和 (填序号),还需补充的仪器是 (填名称)

(2)若补充一种药品还能制取氧气,发生反应的化学方程式为 。
(3)将制取氧气和检验氧气的装置图补充完整。
(4)用排水法收集氧气,当观察到导管口 时,开始收集,气体逸出的原因是由于试管内温度升高且 ,使试管内压强 ,大于外界大气压,在压强差的作用下,气体逸出。
小杨往NaOH溶液中滴加稀硫酸,溶液无明显变化,他和小组同学以“酸与碱能否发生反应”为课题进行了科学探究,请回答下列问题。
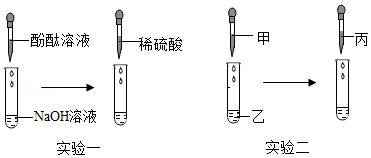
【实验一】
(1)向NaOH溶液中先滴入几滴酚酞溶液,振荡,再滴入稀硫酸,观察到溶液由 色变为无色,该反应的化学方程式为 。
(2)继续往上述试管逐滴滴入NaOH溶液,不断振荡,如果观察到 现象,证明了滴加的稀硫酸过量。
【实验二】按照“证明反应后NaOH消失了”这个角度,同学们又设计了实验二,利用NaOH溶液、CuSO4溶液、稀盐酸同样证明了酸和碱能发生反应,其中试剂丙是 。
【拓展延伸】CO2通入NaOH溶液中也无明显现象,CO2与NaOH溶液能否发生化学反应呢?小组同学对此继续探究。
【查阅资料】常温下NaOH、Na2CO3在水、乙醇中的溶解性如下表所示:
|
溶质 溶解性 溶剂 |
氢氧化钠 |
碳酸钠 |
|
水 |
极易溶 |
易溶 |
|
乙醇 |
易溶 |
微溶 |
【实验三】
小组同学设计了多角度验证CO2与NaOH溶液反应的实验,如实验三图所示(装置已连接好,气密性良好,止水夹a和b已关闭,部分仪器已略去)。
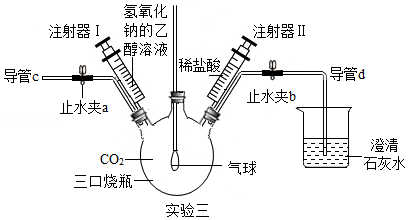
【温馨提示】CO2与乙醇不反应,本实验条件下CO2在乙醇中的溶解忽略不计。
(1)把注射器Ⅰ中氢氧化钠的乙醇溶液注入充满CO2的三口烧瓶中,轻轻振荡,观察到的现象是 。
写出该反应的化学方程式 。
(2)把导管d移出石灰水,打开止水夹a、b,再从导管C端往三口烧瓶中鼓入N2,目的是 。过了一段时间后,先把导管d放入澄清石灰水中,接着关闭止水夹a,再把注射器Ⅱ中的稀盐酸注入三口烧瓶内,观察到三口烧瓶中产生气泡,烧杯中的澄清石灰水变浑浊。此实验从 角度证明了CO2与NaOH溶液发生了反应。
【总结归纳】对于无明显现象的反应,可以通过改变实验装置,创设新的情境,观察到明显的反应现象,从而判断反应的发生。
根据如图回答问题。

(1)A中仪器①的名称是 ,发生反应的化学方程式是 。
(2)B中木条变黑,说明浓硫酸具有 性。
(3)C中会出现明显现象的是试管 (填序号),试管Ⅱ中的蒸馏水需要煮沸、迅速冷却后再使用,目的是 。
梧州市某中学化学兴趣小组的同学查资料知道,乙醇(分子式为C 2H 6O)俗称酒精,通常情况下化学性质稳定,在一定条件下能与氧气反应。现对乙醇与氧气反应进行探究。
【探究活动一】
同学们把绕成螺旋状的红色铜丝在酒精灯的外焰上灼烧到通红,取出铜丝,发现表面变黑,趁热插入装有无水乙醇的试管中(如图),铜丝很快变为红色,并闻到刺激性气味。重复上述操作多次,得到A溶液;经称量,实验前后铜丝质量不变。
铜丝灼烧后生成的黑色物质是 ,铜丝除了给反应加热外,还起到 作用。
【提出问题】生成的刺激性气味的气体是什么?
【猜想与假设】有同学提出刺激性气味的气体可能是:
猜想一:SO 2
猜想二:CO 2
猜想三:醋酸(C 2H 4O 2)
【讨论与结论】同学们讨论后发表看法:
小吴认为猜想一不正确,判断的依据是
小周认为猜想二也不正确,判断的依据是
小施认为猜想三有可能正确,原因是醋酸具有挥发性,并有刺激性气味。
【探究活动二】
小施同学设计实验验证后,发现猜想三也不正确。请补充完成小施的实验操作和现象:取少量A溶液加入试管中,然后 。
【讨论与结论】
老师提示这种刺激性气味气体来源于易挥发的B物质,其相对分子质量为44,且含有C、H、O三种元素(氢元素的质量分数不超过20%),由此可推知物质B的分子式为 。
【拓展活动】
(1)同学们再取少量A溶液加入试管中,加少量无水硫酸铜固体,变蓝色(已知:乙醇、B物质遇无水硫酸铜均不显蓝色),说明乙醇在一定条件下与氧气的反应有 生成。
(2)乙醇在微生物(醋酸菌)作用下与氧气反应能生成醋酸,写出该反应的化学方程式 。

下列是化学实验常用仪器和收集气体装置,回答有关问题:

(1)请写出指定序号的仪器名称:A D
(2)在溶解固体时,C的作用是 ;用B量取液体,读数时视线要与凹液面的 处保持水平。
(3)实验室制取氧气时,用F装置收集氧气,这种收集气体的方法叫 法;不能用E装置收集氧气的原因是 。