梧州市某中学化学兴趣小组的同学查资料知道,乙醇(分子式为C 2H 6O)俗称酒精,通常情况下化学性质稳定,在一定条件下能与氧气反应。现对乙醇与氧气反应进行探究。
【探究活动一】
同学们把绕成螺旋状的红色铜丝在酒精灯的外焰上灼烧到通红,取出铜丝,发现表面变黑,趁热插入装有无水乙醇的试管中(如图),铜丝很快变为红色,并闻到刺激性气味。重复上述操作多次,得到A溶液;经称量,实验前后铜丝质量不变。
铜丝灼烧后生成的黑色物质是 ,铜丝除了给反应加热外,还起到 作用。
【提出问题】生成的刺激性气味的气体是什么?
【猜想与假设】有同学提出刺激性气味的气体可能是:
猜想一:SO 2
猜想二:CO 2
猜想三:醋酸(C 2H 4O 2)
【讨论与结论】同学们讨论后发表看法:
小吴认为猜想一不正确,判断的依据是
小周认为猜想二也不正确,判断的依据是
小施认为猜想三有可能正确,原因是醋酸具有挥发性,并有刺激性气味。
【探究活动二】
小施同学设计实验验证后,发现猜想三也不正确。请补充完成小施的实验操作和现象:取少量A溶液加入试管中,然后 。
【讨论与结论】
老师提示这种刺激性气味气体来源于易挥发的B物质,其相对分子质量为44,且含有C、H、O三种元素(氢元素的质量分数不超过20%),由此可推知物质B的分子式为 。
【拓展活动】
(1)同学们再取少量A溶液加入试管中,加少量无水硫酸铜固体,变蓝色(已知:乙醇、B物质遇无水硫酸铜均不显蓝色),说明乙醇在一定条件下与氧气的反应有 生成。
(2)乙醇在微生物(醋酸菌)作用下与氧气反应能生成醋酸,写出该反应的化学方程式 。

实验室内有一瓶化肥的标签已脱落,只知道它是NH4Cl、(NH4)2SO4和KNO3中的一种.现进行如下实验:
(1)取少量样品在研钵中与 混合研磨,有刺激性气味的气体放出.
(2)另取少量化肥样品与试管中,加入少量水溶解,再滴入图中的 溶液,产生白色沉淀.根据以上实验,可知该化肥为 .
硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂,某同学设计了下列两条途径由废铜料(含铁)生产硫酸铜晶体,其过程如下所示: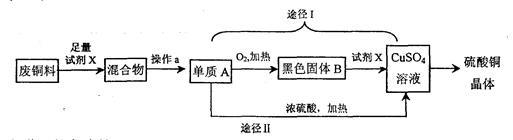
(1)操作a的名称是: ;
(2)已知:Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O。则途径I与途径II相比,其优点体现在:
①不产生二氧化硫有毒气体,不会污染空气;② ;
(3)将废铜料投入硫酸铜溶液中充分搅拌,发生反应的化学方程式为: 。
我国的领海主权不容侵犯。南海是我国的固有领海,蕴藏着丰富的海洋资源。
(1)南海不仅蕴含着大量的煤、石油、天然气等常规化石燃料,还蕴藏着大量的可燃冰。可燃冰(主要成分是CH4)被科学家誉为“未来能源”,CH4燃烧的化学方程式是_______________。可燃冰作为能源与煤、石油相比的优点是___________________________。
(2)南海某岛利用资源优势,建成海水综合利用基地,生产各种产品。
①从海水中获取淡水。目前能规模化和产业化淡化海水的方法主要是_______________。
②从海水中获得氯化钠。将海水进行_________________可得到粗盐。
③从海水中得到金属镁。用苦卤制取金属镁的流程图如下:
苦卤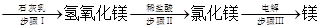
苦卤本身含有MgCl2,又经历了步骤Ⅰ、Ⅱ的转化过程,其目的是_________________;无水MgCl2制取镁的化学方程式为__________________________________。
④以海水中获得食盐为原料制取纯碱。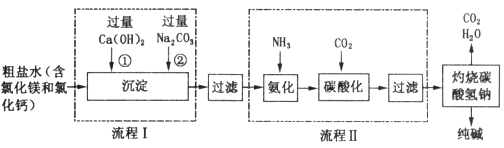
a. 经过流程Ⅰ过滤后得到沉淀是_________________;(填物质的化学式)
b. 流程Ⅱ中发生的总反应为__________________________________;
c. 如果加入氨气不是为了产生氯化铵,那么,氨气在制碱过程中作用是_____________。
氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过以下操作流程: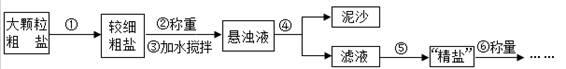
(1)操作①中必须用到的一种仪器是 (填序号)。
A.研钵 B.量筒 C.烧杯 D.试管
(2)小燕完成该实验部分操作过程如图所示,其有明显错误 (填字母序号)。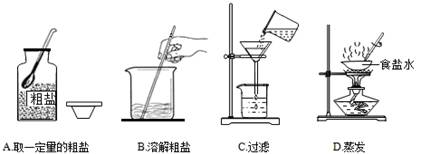
(3)操作⑤中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取 等措施。
(4)实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较低,其可能原因是 (填序号)。
A.食盐没有全部溶解即过滤
B.蒸发时食盐飞溅剧烈
C.蒸发后,所得精盐很潮湿
D.器皿上沾有的精盐没全部转移到称量纸上
(5)小燕查阅相关资料得知:粗盐中除含泥沙等不溶性杂质外,还含有少量的MgCl2、CaCl2等可溶性杂质;为了得到较纯净的氯化钠,小燕将除去泥沙的“精盐”又作了如下处理(假定杂质只有MgCl2、CaCl2两种):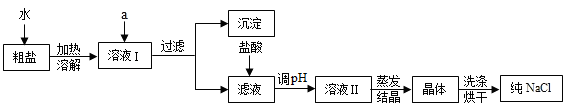
①提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、KOH溶液、饱和NaCl溶液。
从提供的试剂中选出a所代表的试剂是 、 。
②在滤液中加盐酸的作用是 、 (用化学方程式表示)。
(6)井水中也因为含有较多的MgCl2、CaCl2而不能直接饮用,上海世博园内安装的“直饮水”机,采用“活性炭+超滤层+紫外线”净水工艺。活性炭在此起 作用。
(7)已知硫酸钠的溶解度随温度变化的曲线如图所示。40℃时,100g蒸馏水中溶解 g。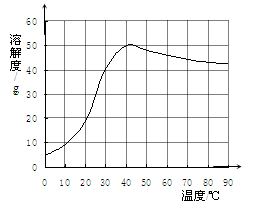
硫酸钠达到饱和。将该饱和溶液升高温度至90℃,观察到的现象是 。
(2014届上海市黄埔区一模试题)草酸(H2C2O4)是一种有机物,在受热条件下分解生成水和另外二种氧化物。某校兴趣小组对此展开探究:
①常用(13) 试剂检验生成物中是否含有水。
②对分解产物中的另外二种氧化物进行假设和验证:(图中固定试管的仪器已略去)
| 假设 |
实验 |
现象 |
结论 |
| 假设一: 生成物中有二氧化碳 |
将生成的气体通入澄清的石灰水 |
现象是 (14) |
生成物中含有二氧化碳。 |
| 假设二: 生成物中有一氧化碳 |
用下图装置进行实验 |
A中的现象是 (15) |
生成物中含有一氧化碳。写出A中的反应化学方程式是(16) |
③下表是根据“假设二”设计的甲、乙两套实验方案,请指出它们各自的不足之处
| 方案 |
步骤 |
不足 |
| 方案甲 |
先通一氧化碳,再点燃酒精灯 |
(17) |
| 方案乙 |
先点燃酒精灯,再通一氧化碳 |
(18) |
查阅资料后同学们改进实验装置如图所示:
该实验过程中装置C的作用是(19)