设计方案是实验探究的保证,感悟方法是探究的根本目的。某合作学习小组开展了如下探究。
实验一:检验氢氧化钠溶液中是否含有氢氧化钙。
【分析】从组成上看,氢氧化钙和氢氧化钠都属于碱,它们在水溶液中都能解离出相同的 (填符号),所以具有相似的化学性质。但由于解离出的Na+和Ca2+不同,所以性质也有不同。设计实验时可加入能解离出CO32﹣的试剂利用CO32﹣与Ca2+结合产生白色沉淀这一特殊现象予以检验。
【设计方案并实验】
实验操作 |
现象 |
结论 |
|
方案一 |
取少量待测溶液于试管中,通入CO2 |
出现白色沉淀 |
氢氧化钠溶液中含有氢氧化钙 |
方案二 |
取少量待测溶液于试管中,滴加 溶液 |
出现白色沉淀 |
写出上述方案中出现白色沉淀的一个化学方程式 。
【方法感悟】在检验物质时,要分析物质的组成和 。据此选择加入恰当的试剂,最后根据不同现象得出结论。
【实验探究】
实验二:有一种白色固体,可能含有氯化钠、氢氧化钠、碳酸钠、硫酸钠和硝酸钡中的一种或几种,为探究其组成,某合作学习小组设计方案并进行了如图实验:
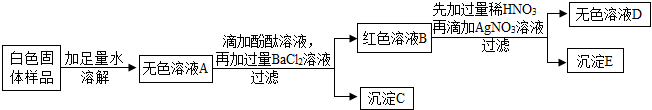
(1)上述实验中,过滤操作用到的玻璃仪器有:烧杯、玻璃棒和 。
(2)小晶同学通过上述实验推知:白色固体样品中一定不含有 。
(3)为确定白色固体样品中可能存在的物质,小燕对沉淀C进行实验。
实验操作 |
现象 |
结论 |
取少量沉淀C于试管中,加入过量 。 |
有气泡产生,沉淀全部消失。 |
白色固体样品中一定含有 。 |
(4)小虎同学认为白色固体中还有物质不能确认其是否存在。其理由是(用化学方程式表示): 。如要确认,只需将上述实验方案中所加的一种试剂改为 即可。
【方法感悟】若其他物质的存在对所检验的物质有干扰时,可先将干扰物质转化,再选择加入恰当的试剂,最后根据不同现象得出结论。
硫酸是化学实验室里的常见试剂.现利用质量分数为98%、密度为1.84g/cm 3的浓硫酸配制100mL质量分数为10%、密度为1.07g/cm 3的稀硫酸.(已知:水的密度近似为1g/cm 3,不同质量分数的溶液混合后总体积不是两种溶液体积之和)
(1)量取浓硫酸时需要的仪器是 .

(2)配制该稀硫酸溶液时,下列方法最合理的是 (假设需要浓硫酸的体积是V mL).
a、分别用量筒量取V mL浓硫酸和(100﹣V)mL水,在烧杯中混合均匀
b、先量取V mL浓硫酸倒入烧杯中,再称量(107﹣1.84V)g水,慢慢倒入盛有浓硫酸的烧杯中混合均匀
c、先量取(107﹣1.84V)mL水倒入烧杯中,再将量取的V mL浓硫酸慢慢倒入盛水的烧杯中混合均匀
d、先在100mL量筒中加入V mL浓硫酸,然后向其中加水恰好至100mL刻度处混合均匀
(3)在量取浓硫酸时若俯视量筒的刻度线,则所配制的硫酸溶液的质量分数 10%(填"大
于"、"等于"或"小于").
(4)用pH试纸测定所配制的硫酸溶液的pH,正确的操作是 .
根据如图所示装置回答下列有关问题:

(1)仪器x的名称是 ;
(2)若用装置B收集氧气,进气口应为 端(选填"a"或"b");
(3)对比装置C和D,可以得出关于可燃物燃烧的条件是 ;
(4)某同学连接A、E、F进行实验,A中所加药品不同,F中所加药品相同.
①若实验时E中蜡烛熄灭,F中溶液变浑浊,则E中现象说明A中产生的气体所具有的性质是 ;
②若实验时E中蜡烛燃烧更旺,F中溶液变浑浊,则A中反应的化学方程式为 .
人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属.硅钢可用于制造变压器的铁芯,某化学兴趣小组的同学为了验证硅钢(主要含有Fe、C、Si),设计了如图的实验流程(有些反应的部分反应物和生成物已省略).
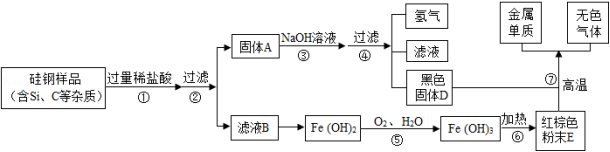
查阅资料发现:常温下,单质硅(Si)不能与盐酸反应,但能与氢氧化钠溶液反应(Si+2NaOH+H 2O═Na 2SiO 3+2H 2↑).
根据以上信息,回答下列问题:
(1)固体A的成分为 ,E的化学式为 ;
(2)滤液B中的金属阳离子为 ;
(3)在过滤操作时,若发现滤液浑浊,应 ;
(4)步骤⑤中发生的是化合反应,尝试写出其化学方程式 .
初中化学中,我们学习了酸和碱发生中和反应的实质是H ++OH ﹣═H 2O.如图,像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式。离子方程式的书写一般按以下步骤:(以Na 2SO 4与BaCl 2反应为例)
①写出Na 2SO 4与BaCl 2反应的化学方程式: ;
②把易溶于水、易电解的物质写成离子形式,把难溶的物质、气体和水等仍用化学式表示。上述方程式可改写成:2Na ++SO 4 2﹣+Ba 2++2Cl ﹣═BaSO 4↓+2Na ++2Cl ﹣
③删去方程式两边不参加反应的离子:Ba 2++SO 4 2﹣═BaSO 4↓
④检查方程式两边各元素的原子个数和电荷总数是否相等。
请回答:
(1)下列各组中的离子,在pH=3的水溶液中能大量共存的是
A、Na +、Mg 2+、Cl ﹣、SO 4 2﹣ B、Na +、K +、Cl ﹣、OH ﹣
C、Na +、Cu 2+、Cl ﹣、SO 4 2﹣ D、Na +、K +、Cl ﹣、CO 3 2﹣
(2)写出稀盐酸滴在石灰石上所发生反应的离子方程式 ;
(3)写出一个与离子方程式Mg+2H +═Mg 2++H 2↑相对应的化学方程式 ;
(4)酸、碱、盐在水溶液中发生的复分解反应实质上就是两种化合物在溶液中相互交换离子的反应,只要具备生成物中有气体或沉淀或 生成,反应就能发生。

我市著名的纸面石膏板企业,用热电厂燃烧煤产生的炉渣来生产石膏板.原理是:发电过程中产生的烟气中含有大量的SO 2,热电厂用"碱﹣石灰﹣石膏(CaSO 4•2H 2O)"的方法使烟气脱硫从而生成石膏.
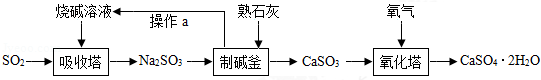
(1)工业烟气没经处理直接排放到空气中易形成 ,会污染、破坏环境;
(2)写出吸收塔内发生反应的化学方程式 ;工业上用分离液态空气法制氧气,是利用空气中各成分的 不同进行分离的;
(3)化学反应类型有不同的分法,其中反应前后,有元素化合价变化的化学反应是氧化还原反应.有元素化合价升高的反应物是还原剂,有元素化合价降低的反应物是氧化剂.化学反应前后元素化合价没有变化的化学反应是非氧化还原反应.则下列说法正确的是
A、吸收塔、制碱釜中发生反应属于氧化还原反应
B、制碱釜中的反应物Na 2SO 3作氧化剂
C、氧化塔中发生的反应属于氧化还原反应
D、氧化塔中的反应物CaSO 3作还原剂
(4)生产流程中生成的 可循环利用,节约成本.