汽车尾气催化转换器可减少有害气体的排放,其中某一反应过程的微观变化如图所示。请回答下列问题:
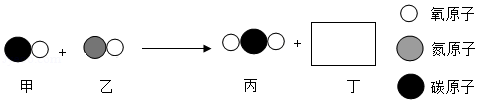
(1)化学反应前后:物质总质量是否发生改变? (选镇"是"或"否");种类发生改变的微粒是 ( 选填"分子"或"原子")。
(2)丙微粒中碳元素的化合价为 。
(3)已知丁是一种单质,则丁是 ( 写化学式)。
(4)该反应的化学方程式为 。
请根据如图实验回答问题。

(1)图一为测定空气里氧气含量的实验。点燃红磷前,需要用弹簧夹夹紧胶皮管的原因是 。 该实验中不能用铁丝代替红磷的原因是 。
(2)图二为探究分子性质的实验。实验中观察到烧杯B中的液体由无色变为红色,说明分子具有的性质是 。
(3)图三为探究固体溶解时的热量变化实验,若向试管中加入的固体是NH4NO3,可观案到U形管内左侧液面 (填“低于”或“高于”)右侧液面。
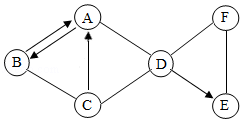
A﹣F为初中化学中常见的六种物质,其中A、B、C、D、E为五种不同类别的物质,A为大理石的主要成分,其相互反应及转化关系如图所示。(图中“﹣”表示相连的物质间能相互发生反应,“→”表示物质间有相应的转化关系,部分反应物、生成物及反应条件已略去)。请回答。
(1)C物质的一种用途是 。
(2)D→E的基本反应类型为 。
(3)B→A的化学方程式为: 。
(4)F的化学式可能是 。
金属材料广泛应用于生活和生产中。
(1)下列物品所用的主要材料属于金属材料的是 (填字母)。
A.瓷碗 B.玻璃瓶 C.一元硬币 D.硬铝门窗
(2)生铁和钢是使用最多的金属材料,二者性能不同的原因是 。 工业上采用赤铁矿石(主要成分为氧化铁)炼铁的反应原理是 (用化学方程式表示)。
(3)向Al(NO3)3、Cu(NO3)2、和AgNO3的混合溶液中加入一定量铁粉,待充分反应后过滤,向滤渣中加入稀盐酸。
①若有气泡产生,则滤液中的溶质是 ;
②若没有气泡产生,则滤液中溶质的组成最多有 种情况。
如图是某品牌的风味酸牛奶及每100g酸牛奶中主要营养成分数据。请回答下列问题。
|
营养成分 |
蛋白质 |
脂肪 |
糖类 |
钠 |
钙 |
|
质量 |
3.2g |
3.6g |
11.9g |
60mg |
80mg |
(1)人体必需的六大类基本营养素中,除水外,表中没有标示的营养素是 。
(2)表中能为人体提供能量的营养素有 种。
(3)该酸牛奶的外包装是一种塑料制品,随意丢弃会造成“白色污染”。为减少“白色污染”,可采取的措施是 (答一点)。
(4)酸牛奶中的蔗糖,在胃肠内转化为葡萄糖(C6H12O6)。葡萄糖在酶的催化作用下,与氧气反应生成水和二氧化碳,请写出该反应的化学方程式 。

小明同学欲测定某纯碱样品(含少量氯化钠)中碳酸钠的质量分数,取26.5g该纯碱样品加入到100g水中,使其完全溶解,再加入169.3g稀盐酸,恰好完全反应,得到287g不饱和溶液。请计算:
(1)纯碱样品中碳酸钠的质量分数
(2)反应后得到的不饱和溶液中溶质的质量分数。