某化学兴趣小组为测定某有机物(含C、H、O三种元素)中各元素的质量比,用如图实验装置(部分夹持装置略去)进行探究。

提示:装置C中发生的反应为2Na2O2+2CO2=2Na2CO3+O2
实验数据:
读数 |
反应前质量/g |
反应后质量/g |
电子天平a |
217.0 |
222.4 |
电子天平b |
150.0 |
158.4 |
请计算该有机物中各元素的质量比(写出计算过程)。
圆梦中学现有20%的硝酸钾溶液、蒸馏水、硝酸钾固体,现需要100g质量分数为15%的硝酸钾溶液,请根据下列要求计算:
(1)若选用硝酸钾固体和蒸馏水来配制,各需多少?
(2)若选用20%的硝酸钾溶液与蒸馏水来配制,各需多少?
汽车蓄电池中稀硫酸的溶质质量分数为28%,密度为1.2g/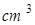 。若要在实验室用溶质质量分数为98%的浓硫酸配制这种稀硫酸630g。求:
。若要在实验室用溶质质量分数为98%的浓硫酸配制这种稀硫酸630g。求:
(1)630g稀硫酸的体积是多少毫升?
(2)需要浓硫酸多少克?
现有10%的硝酸钾溶液160g,分为质量相等的两份.
(1)欲使其中一份溶质的质量分数增大一倍,求:
①若用增加溶质的方法,需增加多少克硝酸钾?
②若用蒸发溶剂的方法,需蒸发多少克水?
③若用60%的硝酸钾溶液与其中一份混合的方法,需要加入60%的硝酸钾溶液多少克?
(2)欲使其中一份溶质的量分数变为5%,需要加水多少克?
26g黄铜(Cu—Zn合金)与100g稀硫酸在烧杯中恰好完全反应,反应后测得烧杯中剩余物的总质量为125.8g.求:(1)黄铜中铜的质量分数;(2)反应后所得溶液中溶质的质量分数.(计算结果精确到0.1%)
为测定Cu—Zn合金的组成,小华同学利用该合金粉末与稀硫酸反应,进行了三次实验,所得相关实验数据记录如下:
| 第一次 |
第二次 |
第三次 |
|
| 所取合金的质量/g |
10 |
10 |
20 |
| 加入硫酸的质量/g |
50 |
80 |
50 |
| 生成氢气的质量/g |
0.2 |
0.2 |
0.2 |
请计算:
(1)从上表数据分析,当所取合金与所用稀硫酸的质量比为________时,表明合金中的锌与稀硫酸恰好完全反应;
(2)10g该合金中锌的质量为多少克?(计算结果保留一位小数)
(3)所用合金中的锌与稀硫酸恰好完全反应时所得溶液中溶质的质量分数为多少?(计算结果精确到0.1%)