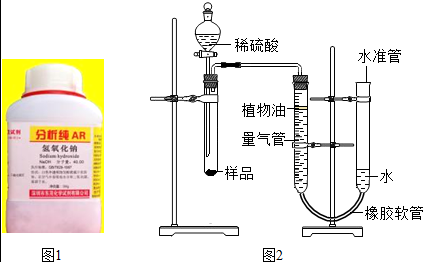
实验室有一瓶长期放置的氢氧化钠固体(如图1),某兴趣小组同学欲对该固体变质情况进行探究。
【提出问题】该瓶氢氧化钠固体是否变质,变质情况如何?
【查阅资料】①氢氧化钠在空气中容易变质但不会转化为NaHCO 3;
②CaCl 2溶液呈中性
③CaCl 2+Na 2CO 3═CaCO 3↓+2NaCl
【提出猜想】猜想Ⅰ:固体未变质
猜想Ⅱ:固体全部变质
猜想Ⅲ:固体部分变质
【原因分析】氢氧化钠在空气中变质的原因是 (用化学方程式表示)。
【进行实验】小聪同学取少量样品于烧杯中,用足量水溶解,再向溶液中滴入几滴酚酞试液,溶液变红,由此他得出猜想Ⅰ正确,但其他同学很快予以否定,否定的理由是 ,为了进一步得出结论,组内其他三位同学分别取小聪实验后的溶液于试管中,进行如下表所示实验。
同学 |
小红 |
小美 |
小伍 |
实验操作 |
加入适量氢氧化钙溶液 |
加入过量氯化钙溶液 |
加入过量稀盐酸 |
【实验结论】小红、小美的实验中都观察到有白色沉淀生成且溶液仍是红色,于是他们都出猜想Ⅲ正确。
【反思评价】(一)老师指出,仅凭小红的实验操作和现象无法确定猜想Ⅲ正确,理由是 。
(二)根据小美的结论推测小实验现象是 。
【提出问题】如何测定变质的氢氧化钠固体中碳酸钠的质量分数?
【实验原理】通过测定一定质量样品与足量稀硫酸反应生成二氧化碳的体积来计算碳酸钠的质量分数。
【实验设计】小伍称取一定质量的样品,按如图2装置进行实验(已知该装置气密性良好,水准管高度可以上下调节,量气管是带有刻度的仪器)。
【反思评价】(一)在实验中,若没有植物油,测定结果会 (填"偏大"、"偏小"或"不变")。
(二)操作中,下列情况不影响测定结果的是 (填字母)。
A、实验前试管中有空气
B、实验中水准管口有水溢出
C、读数时量气管和水准管液面不相平
D、实验后生成的气体在试管中仍有滞留。
化学是一门以实验为基础的科学。根据下列实验装置图,回答有关问题:

(1)实验室用装置A制取氧气时,试管中所盛的药品是_____,若用装置D收集产生的氧气,气体应从_____(填“a”或“b”)端进入。
(2)实验室用锌与稀硫酸制取氢气时,反应的化学方程式为_____,如果用装置E检验氢气,现象是_____。
(3)实验室用装置B制取二氧化碳时,反应的化学方程式为_____,装置C也可作为实验室制取二氧化碳的发生装置,与装置B相比,选用装置C的优点是_____。二氧化碳溶于水形成碳酸,用装置F检验其酸性时的现象是_____,图中标有①的仪器名称是_____。
脱氧剂可以延长食品保质期。某脱氧剂的主要成分为铁粉、活性炭和氯化钠。针对该脱氧剂进行如下活动:
活动一:验证脱氧剂中含有铁粉和活性炭
【进行实验】
(1)取脱氧剂样品于试管中,加入足量的稀盐酸,观察到有气泡产生,溶液变为浅绿色,说明脱氧剂中含有铁粉。写出该反应的化学方程式__________;
(2)充分反应后,将试管中的固液混合物过滤,将滤渣洗涤、干燥,得到黑色固体;
(3)如图所示,将黑色固体置于坩埚(耐高温容器)内,在电炉上灼烧,最终黑色固体全部消失。灼烧期间,在坩埚上方罩上烧杯,过一会儿,迅速把烧杯倒过来,向烧杯内注入澄清石灰水,振荡,观察到__________的现象,说明脱氧剂中含有活性炭。
【反思与评价】用酒精灯替换电炉重复(3)实验,虽出现相同现象,但会影响实验结论,其原因是__________。
活动二:探究脱氧剂中氯化钠的作用
【查阅资料】脱氧剂能延长食品保质期是利用了铁生锈的原理
【猜想与假设】氯化钠可能影响铁生锈的速率
【进行实验】按如图所示A、B装置进行实验,相同温度下,每隔一段时间测量导管中水面上升高度,实验数据如下表。
|
时间/ |
|
|
|
|
|
A装置导管中水面上升高度/ |
|
|
|
|
|
B装置导管中水面上升高度/ |
|
|
|
|

【解释与结论】
(1)从化学、物理两个视角综合分析,A、B装置导管中水面上升的原因是__________;
(2)结合表中数据,得出脱氧剂中氯化钠的作用是_____(填“加快”或“减慢”)铁生锈的速率。
【拓展与应用】铁生锈的原理在生活中有诸多应用
(1)取暖用的“暖宝宝”主要成分与脱氧剂相同,说明铁生锈是_____填“吸热”或“放热”)反应;
(2)写出一种防止铁生锈的具体方法_____。

可控的火是福,不可控的火是祸。如图是利用对比法探究燃烧条件的实验装置,回答下列问题:(已知:白磷的着火点为 ,红磷的着火点为 )

(1)图1中薄铜片上的白磷燃烧而红磷不燃烧,说明燃烧需要的条件是__________;
(2)图1中薄铜片上的白磷燃烧而水中白磷不燃烧,说明燃烧需要的条件是__________;
(3)磷燃烧的生成物有毒。与图1装置相比,利用图2装置进行实验的优点是__________。
“天宫课堂”上航天员做的泡腾片实验,让同学们再次感受到化学的魅力。泡腾片中含有碳酸钠或碳酸氢钠等物质,化学兴趣小组决定对它们的某些性质进行探究。
实验一:探究碳酸钠和碳酸氢钠溶液的酸碱度
【实验探究1】用pH试纸测得等浓度的碳酸氢钠溶液的pH为9,碳酸钠溶液的pH为11。
【实验结论1】两者均显碱性,且溶液碱性较强的是 。
实验二:探究碳酸钠和盐酸的反应
【实验探究2】向盛有碳酸钠溶液的烧杯中,逐滴加入一定浓度的稀盐酸并充分搅拌,测得pH变化与时间的关系如图1所示。观察到ab段无气泡产生,从b点开始产生气泡。经测定b点溶质只有碳酸氢钠和氯化钠,c点pH为7。

【实验结论2】碳酸钠和盐酸的反应是分两步发生的,ab段发生反应的化学方程式为 ,c点溶液中的溶质为 。
实验三:探究碳酸钠和碳酸氢钠的热稳定性
【查阅资料】①碳酸氢钠受热分解成碳酸钠、水和二氧化碳;②碳酸钠受热不分解。
【实验验证】取一定量的碳酸氢钠放入试管中加热,如图2所示。

【交流反思】试管A管口向下倾斜的原因是 ,试管B中出现 现象,证明有二氧化碳生成。
【实验结论3】碳酸钠的热稳定性强于碳酸氢钠。
【拓展应用】溶洞内钟乳石的形成原理与碳酸氢钠受热分解相似﹣﹣溶有碳酸氢钙[ ]的地下水,遇热或当压强突然变小时,碳酸氢钙会分解成碳酸钙沉积下来,天长日久就形成了千姿百态的钟乳石。请写出碳酸氢钙分解的化学方程式 。
实验室配制50g质量分数为6%的NaCl溶液,配制过程包括如下操作。请回答:

(1)图中使用到的玻璃仪器有 、量筒、玻璃棒、广口瓶四种。
(2)溶解时用玻璃棒搅拌的目的是 。
(3)该实验中量取的水的体积应为 mL。(水的密度为 )
(4)图示中正确的操作顺序为 (填标号)。
| A. |
④②⑤①③ |
| B. |
①②③④⑤ |
| C. |
①②④③⑤ |
| D. |
④⑤②③① |