某化学兴趣小组通过探究活动学习和理解化学知识.请你一起研究学习,并回答有关问题.
研究主题:水溶液中复分解反应的实质
相关信息:一定体积的溶液中,离子的数目越多,其离子的浓度越大.电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小.相同温度下同种溶液电导率越大,离子浓度越大.
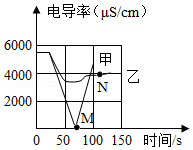
(1)实验一:恒温条件下,向一定体积一定浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀硫酸,测得溶液的电导率变化如图中甲曲线所示.
①写出Ba(OH)2与H2SO4反应的化学方程式 .
②甲曲线M点时混合液体呈 色;
③通过对甲曲线的分析,下列说法错误的是 (填序号).
A.M点前曲线下滑的过程中,H+和OH﹣结合成H2O,Ba2+和SO42﹣结合成BaSO4
B.M点时离子浓度几乎为零
C.M点后溶液电导率逐渐增大,仅由于溶液中H+在逐渐增大
(2)实验二:恒温条件下,向等量同浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀Na2SO4溶液,测得溶液的电导率变化如上图乙曲线所示.
①通过对乙曲线的分析,下列说法错误的是 (填序号).
A.开始至完全反应过程中,电导率减小,溶液由红色逐渐变为无色
B.电导率下降到最低点时仍然较大,表明溶液中还存在较多离子
C.整个实验过程中,溶液中Na+数目一直增大
②N点时,溶液中含有的离子是 (填离子符号).
③通过比较分析,结合已学知识可知,溶液中复分解反应的实质是参与反应的离子,结合生成了沉淀、气体或水,导致其浓度 (填“增大”或“减小”).
(3)拓展:①请根据示例仿写离子方程式.
示例AgNO3+NaCl=AgCl↓+NaNO3离子方程式:Ag++Cl﹣=AgCl↓
仿写:BaCl2+Na2SO4=BaSO4↓+2NaCl离子方程式: .
②向一定量饱和澄清石灰水中持续通入过量的CO2气体,溶液先变浑浊后浑浊逐渐消失.请推测此过程的溶液中Ca2+的浓度变化情况 .
小明发现家中一枚戒指生满了铜绿,他和同学利用这枚戒指展开了研究性学习。
【查阅资料】真金在空气中不会生锈,生满铜绿的“金戒指”材质为铜锌合金;铜长期露置在潮湿的空气中能生成铜绿,其主要成分是碱式碳酸铜,碱式碳酸铜受热易分解生成CuO、H2O和CO2。据上述资料可推知,碱式碳酸铜由种元素组成。
【实验探究】将该枚戒指加入过量稀盐酸中,有气泡产生,溶液由无色逐渐变为蓝绿色。
(1)小明认为:气体中除了含有CO2,还可能含有少量。实验室常用的方法检验这种可能含有的气体。
(2)小红认为,除了水外,蓝绿色溶液中只含有氯化锌。小华认为除了水和氯化锌外,蓝绿色溶液中还应该含有、。他取适量上述蓝绿色溶液,加入光亮的铁片,观察到了现象:① ,② ,证实了自己的观点。
(3)小娟取适量新制的FeCl2溶液,加入锌粒,一段时间后,溶液颜色变浅。结合小华的实验可推知:铁、锌、铜三种金属的活动性由弱到强的顺序是。
(4)小明想进一步探究“金戒指”中铜元素的含量,取一枚同材质的“金戒指”,称得质量为3.8g。在老师的指导下,将“金戒指”经浓硝酸氧化、碱化等步骤处理后,最终得到纯净的氧化铜,称得质量仍然为3.8g(实验过程中铜元素损失忽略不计)。则“金戒指”中铜元素的质量分数是多少?(写出计算过程)
近几年,我国酸雨污染较为严重,在2007年监测的500个城市中,出现酸雨的城市有281个,占56.2%。有关资料显示,我国的酸雨主要是因为大量燃烧含硫量高的煤而形成的(在我国的能源结构中,燃煤约占70%),此外,各种机动车排放的尾气也是形成酸雨的重要原因。
【提出问题】通过实验证明煤中含有碳元素和硫元素。
【查阅资料】① “二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),该反应的化学方程式为:5SO2 + 2KMnO4 + 2H2O="==" K2SO4 + 2MnSO4 + 2  ” 。资料上这个化学方程式中最后一种物质的化学式印刷不清楚,请推测其化学式:。在上教版九年级化学教材中即用此原理检验含硫火柴中的硫元素。
” 。资料上这个化学方程式中最后一种物质的化学式印刷不清楚,请推测其化学式:。在上教版九年级化学教材中即用此原理检验含硫火柴中的硫元素。
② “二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊。”请书写该反应的化学方程式:
。
根据上述资料,甲同学和乙同学分别设计实验方案进行探究。
(1)甲同学:
【进行实验】甲同学进行了如下图所示A、B两步实验:
【观察现象】高锰酸钾溶液褪色,澄清石灰水变浑浊。
【得出结论】煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
你认为该实验方案是否合理并简述理由:。
(2)乙同学:
【进行实验】乙同学进行了如下图所示实验(部分装置在图中略去):
B装置的作用是,C装置的作用是。
【观察现象】。
【得出结论】煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
兴趣小组同学为了弄清沼气池中气体的成分,进行了有关实验。请你与他们一起完成以下探究活动(已知氢氧化钠溶液能吸收二氧化碳气体):
【收集气体】将不加盖的矿泉水瓶装满水,用细绳吊入池中,再用木棍拨动使瓶中的水全部倒出(见右图),然后迅速拉起矿泉水瓶,盖上瓶盖。这种方法属于集气法。
【对气体猜想】
猜想Ⅰ.全部是CH4;猜想Ⅱ.全部是CO;
猜想Ⅲ.全部是CO2;猜想Ⅳ.是CH4和CO2的混合气体。
【实验和推断】
(1)若“现象a”为石灰水变浑浊,则说明气体中含有气体。
(2)步骤②的目的是;步骤③“注水装置”应选右图中的(填序号)。
(3)若“现象b”为杯壁有水雾出现,有同学认为“猜想Ⅰ或Ⅳ”成立,其反应方程式为:
。另有同学认为此现象不能证明收集到的气体中一定含有氢元素,理由是;要排除这种干扰可采取的措施是。
(4)采取(3)中的排除干扰措施后,若“现象a、c”均为石灰水变浑浊,“现象b”为杯壁有水雾,则证明“猜想”成立(填序号)。
今年地球日主题为:“珍惜地球资源,转变发展方式”。为减少化石燃料的使用,降低污染,各国都在积极进行技术创新。
(1)美国科学家发明了一种“发电叶子”,将这种叶子放入水中,在太阳光照射下,叶子中的催化剂会将水分解成氢气和氧气储存在氢氧燃料电池中,再转化为电能,供家庭用电需求。
①整个过程中都发生了哪些形式的能量转化:。
②“发电叶子”产生氢气、氧气的化学方程式为。
(2)我国积极改进风电技术,扩大风电使用,并配套大型储能设备——“全钒液流”储能电池,以保证稳定供电。
①与煤炭火力发电相比,风力发电的优点是。
②“全钒液流”储能电池在充电时,电池中的VO2+会变成VO2+,这个过程中钒元素(V)的化合价由价变为价。
(3)为了降低汽车排放的尾气对空气的污染,现在的大部分汽车都安装了催化式排气净化器。下图列举的是几种气体在净化器中转换前后的变化。
①根据下图所提供的信息,举例说明催化式排气净化器是如何降低汽车尾气污染的:
。
②气体在催化式排气净化器里面发生了化学变化。请用原子、分子的知识概括化学变化的实质:。
③为了使汽车尾气的污染更小,研究催化式排气净化器的专家们还要注意什么问题:
。
某化学小组围绕燃烧与灭火的主题开展了相关活动。请你参与完成: 【知识回忆】可燃物燃烧的必备条件是、。
【知识回忆】可燃物燃烧的必备条件是、。
【交流讨论】(1)改进后的装置(如图二)与图一相比,其优点是。欲使图二中的红磷着火,可将试管从水中取出并后才能对试管加热;
(2)将装有某气体的大试管口朝下垂直插入水中,使试管罩住白磷(如图三),结果观察到了“水火相容”的奇观,则大试管所装气体可能是;
【综合应用】“水火不相容”是指水能灭火,其实水有时也可以“生火”,比如钾遇水会立刻着火,因为钾遇水生成氢气和一种叫氢氧化钾的物质,该反应是(填“吸热”或“放热”)反应,其反应化学方程式为。