工厂的烟气脱硫工艺,不仅能消除二氧化硫,还能将其转化为硫酸钙(CaSO 4)等产品,实现"变废为宝".反应的化学方程式为:2CaCO 3+O 2+2SO 2 2CaSO 4+2CO 2,现用1.25t含碳酸钙80%的石灰石吸收烟气中的二氧化硫.求:
(1)石灰石中碳酸钙的质量.
(2)可吸收二氧化硫的质量.
乙醇(C2H5OH)可用作燃料。按要求计算:
(1)乙醇分子中C、H、O原子个数比为 ;
(2)乙醇中碳元素和氢元素的质量比为 (写最简比);
(3)乙醇的相对分子质量为 ;
(4)9.2g的乙醇中含有碳元素的质量为 g。
某固体混合物中可能含有氢氧化钠、硝酸钠、氯化钠,硫酸钠、碳酸钠。为了研究该混合物的成分,某同学按下列流程进行了实验(各步均恰好完全反应):
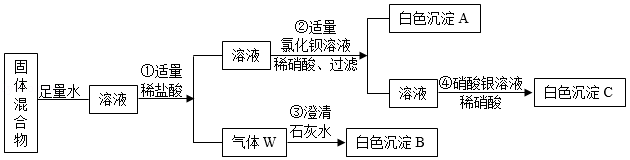
根据流程图回答问题:
(1)反应③的化学方程式为 ,反应④的化学方程式为 。
(2)根据实验现象推断该混合物中一定含有的物质是 (填化学式)。
(3)该同学为了进一步确定固体混合物的组成,取样品20.9g(其中含钠元素质量为6.9g),按上述流程图进行实验,产生11.65g白色沉淀A,产生2.2g气体W.通过计算,确定该混合物中还含有的物质是 (填化学式),其质量为 g。
金属具有广泛的应用。
(1)铁锅用来炒菜,主要是利用铁的 性(填“导热”或“导电”)。
(2)图为洁净铁钉的有关实验。

①中铁与硫酸铜反应的化学方程式为 。
②中铁钉锈蚀主要是铁与空气中的氧气和 发生化学反应。
③中铁锈与稀硫酸反应的化学方程式为 。
(3)某炼铁厂要冶炼1000t含杂质3%的生铁,需要含Fe2O380%的赤铁矿石的质量是 t(计算结果精确至0.1t)。
(4)某金属粉末可能由镁、锌、铁、铝、银中的一种或几种组成。取该样品2.4g,向其中加入100g一定溶质量分数的稀硫酸,恰好完全反应,生成0.2g氢气,得到无色溶液,固体无剩余。下列说法正确的是 (填序号)。
A.样品中一定含有镁
B.样品中一定不含有银,可能含有铁
C.所得溶液中溶质总质量为12g
D.加入的稀硫酸的溶质质量分数为19.6%
根据下列装置图回答问题。
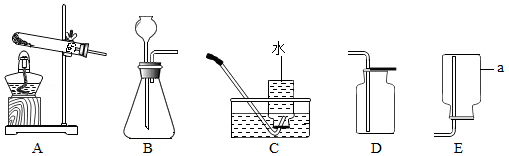
(1)写出仪器a的名称: 。
(2)实验室用加热高锰酸钾的方法制取并收集氧气,应选用的装置为 (填序号),该反应的化学方程式为 。
(3)实验室用石灰石和稀盐酸反应制取并收集二氧化碳,应选用的装置为 (填序号),该反应的化学方程式为 。
(4)实验室制取气体时,连接好仪器装置,在装入药品前要检查装置的 。
溶液与人类生产、生活密切相关。
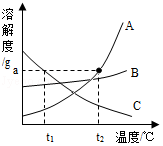
(1)A、B、C三种固体物质的溶解度曲线如图所示。
①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是 。
②A、B、C三种物质中,溶解度随温度升高而减小的是 。
③t2℃时,完全溶解agA物质最少需要水的质量是 g。
④t2℃时,相同质量的A、B饱和溶液中,A的饱和溶液中所含水的质量 B的饱和溶液中所含水的质量(填“大于”、“等于”或“小于”)。
(2)实验室欲除去粗盐样品中含有的不溶性泥沙,在过滤操作中需要用到的实验仪器和用品有:烧杯、铁架台(带铁圈)、玻璃棒、 和滤纸。
(3)在实验室中,配制溶质质量分数为10%的氯化钠溶液45g,需要氯化钠固体的质量是 g.将45g10%的氯化钠溶液配成含氯化钠为0.9%的溶液,得到氯化钠溶液的质量是 g。