某校化学兴趣小组在学完碱的化学性质后,做了澄清石灰水和稀盐酸反应的实验,并将废液倒入一洁净的废液缸中,进行了如下探究:
探究Ⅰ:甲同学在做实验时没有观察到明显现象,于是对澄清石灰水和稀盐酸能否发生反应表示怀疑,乙同学认为,甲同学实验时应先向澄清石灰水中滴几滴酚酞试液,再滴加适量的稀盐酸,当观察到 时,就可以说明两种物质能发生反应。
探究Ⅱ:废液中溶质的成分是什么?
[做出猜想]
猜想一:CaCl2
猜想二:CaCl2、HCl
猜想三:CaCl2、HCl、Ca(OH)2
你的猜想:
丙同学认为猜想三是错误的,理由是 (用化学方程式解释)。
[实验设计]
设计者 |
实验操作 |
实验现象 |
实验结论 |
丁同学 |
取少量废液于一支试管中,向其中加入足量的碳酸钠溶液 |
有白色沉淀生成 |
猜想一正确 |
戊同学 |
取几粒锌粒于一支试管中,向其中加入少量废液 |
|
猜想二正确 |
[评价与反思]请判断以上设计的两个方案中, 同学的方案合理,请分析另一个方案不合理的理由: 。
[表达与交流]若实验证明猜想二是正确的,你认为该废液未经处理直接倒入下水道,可能造成的危害是 (填一点)。
某校进行九年级化学实验技能考查,确定了以下三个考题:①粗盐提纯;②实验室制取和收集二氧化碳;③实验室制取和收集氧气.考查规定由学生抽签确定考题.
甲同学抽签后被监考老师引导至准备了下列仪器和药品的实验台前:
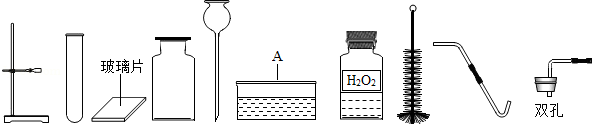
(1)如图中仪器A的名称是 ;分析抽签确定的考题,甲同学发现其中缺少了一种药品,向老师申请补充后完成实验.请写出该实验的化学反应方程式 .
(2)以下是甲同学实验时的主要步骤,这些步骤的正确顺序是 (填字母标号).
A.制备气体 B.收集气体
C.检查装置的气密性 D.清洗仪器,整理试验台
若另选药品,也能完成另一个考题,发生的化学反应方程式为 .
根据所学化学知识完成下列问题:
(1)请从分子角度解释:八月桂花,十里飘香.
(2)资源是有限的,金属资源的回收和利用很重要,请谈谈回收和利用的价值所在. .
小明同学设计以下实验来探究可燃物燃烧的条件和测定空气中氧气的含量.(已知:白磷的着火点是40℃,红磷的着火点是240℃)
|
实验装置 |
实验过程 |
实验现象 |
|
|
①取一烧杯,加入适量的生石灰,再分别取少量白磷、红磷放在烧杯上的铜片上. ②… |
一会儿白磷发生燃烧,红磷不燃烧 |
|
|
③先在容积为350mL的集气瓶中装进50mL滴有红墨水的水,在燃烧匙中放足量白磷,量筒中盛入足量水. ④按图连好仪器,用激光手电照射白磷,白磷燃烧. |
集气瓶和量筒中的水均为红色,量筒内的液体体积减少约60mL |
(1)实验过程②是 ,烧杯中发生反应的化学方程式为 ;
(2)白磷燃烧反应的化学方程式为 ;
(3)根据实验2的结果,计算空气中氧气的体积分数约为 (写出计算式和结果);
(4)在整个实验2的过程中,集气瓶内的压强变化是 ,集气瓶中预先装入50mL水,水起的作用是 .
小苏打常用作焙制糕点的发酵剂,为测定某小苏打样品的纯度,现取样品10g加热到质量不在减少(杂质不参加反应),共收集到二氧化碳2.2g,求样品中小苏打的纯度。提示:碳酸氢钠受热分解的化学方程式:2NaHCO3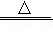 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
(1)六盘水市四创主题之一是"创建生活宜居城市",下列符合该主题的是
A.植树造林、美化环境 B.为解决白色污染,将塑料收回利用 C.鼓励使用太阳能热水器
(2)先进的交通工具可以使出行更便捷,沪昆高铁是国家铁路交通额重要组成部分,预计2016年年底建成通车,六盘水市将步入"高铁时代".列出制造离不开下列材料:A.金属材料 B.合成材料 C.复合材料
根据要求选择填空(填序号):
①列车制造中需要大量的钢铁,钢铁属于 .
②高铁座椅需用到耐磨、耐腐蚀的涤纶等材料,涤纶属于 .
(3)水是生命之源,万物之基,是人类宝贵的自然资源,我们每个人都要珍惜水、爱护水、节约用水,请举一例说明生活中你是如何节约用水的: .