将含有NaCl杂质的某烧碱样品10g完全溶于90g水中,再向所得溶液中慢慢滴入溶质质量分数为7.3%的稀盐酸.在实验过程中,溶液的pH与滴入稀盐酸的质量关系如图所示.
(1)求l0g该样品中氢氧化钠的质量.
(2)求a点时,溶液中溶质的质量分数(计箅结果精确到0.1%)

如图所示是几种实验室制取气体的发生装置和收集装置:

回答下列问题:
(1)写出图中标有数字的仪器名称: 。
(2)实验室用石灰石和稀盐酸制取二氧化碳,发生装置可选用图中的 装置(填字母序号),写出该反应的化学方程式: 。
(3)实验室用氯酸钾与二氧化锰制取氧气,若要使收集到的氧气较为纯净,最好选用图中的 装置进行收集(填字母序号)。
在研究“酸碱中和反应”时,某兴趣小组同学想证明稀盐酸与氢氧化钠溶液混合后是否发生了化学反应,进行了如下探究:
(1)在盛有氢氧化钠的溶液的烧杯中滴入几滴酚酞溶液,再逐滴加入稀盐酸,并不断搅拌(如图一)。用数字化传感器测得盐酸与氢氧化钠溶液混合前后的温度变化情况(如图二)。
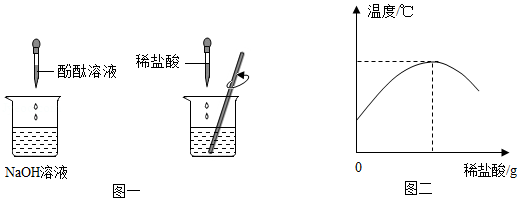
由实验现象和曲线变化情况分析可知,盐酸和氢氧化钠溶液发生了反应并 (填“吸收”或“放出”)热量。
(2)从微观角度分析盐酸与氢氧化钠溶液的反应
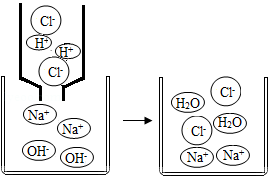
由如图可知,该反应的微观实质是 。
[交流讨论]同学们讨论后认为,如果盐酸和氢氧化钠减少(或消失),或者有新物质生成,都能证明反应已经发生。
(3)探究实验后烧杯中溶质的成分。
|
步骤 |
现象 |
结论 |
|
实验1:取烧杯中的溶液少许于试管中,加入硫酸铜溶液 |
|
证明没有NaOH |
|
实验2:另取烧杯中的溶液少许于试管中,加入硝酸银溶液 |
出现白色沉淀 |
证明含有HCl |
|
实验3:再取烧杯中的溶液少许于蒸发皿中,加热蒸干 |
有 产生 |
证明有NaCl生成 |
[得出结论]氢氧化钠溶液和盐酸发生了中和反应。
[评价反思]
Ⅰ.有同学认为,仅通过实验2出“溶液中含有HCl”证据不足,理由是 。
Ⅱ.运用中和反应,可以解决生产,生活中的实际问题。如工厂用氨水(NH3•H2O)处理废水中的硫酸,能得到一种氮肥一硫酸铵,写出该反应的化学方程式 。
Ⅲ.多角度认识化学反应是学习化学的重要方法。
某固体物质中可能含有NaCl、BaCl2、NaOH中的一种或几种。某校课外小组同学为了探究其成分,取该固体物质30g完全溶于水中,测得溶液的pH为7,然后将70g某稀硫酸加入该溶液中,充分反应,所加硫酸的量与产生沉淀的关系如图所示。请根据图示及相关知识回答问题。
(1)该固体物质中一定不含有的物质是 (化学式)。
(2)通过计算确定固体物质的组成成分及质量。
(3)这种稀硫酸中溶质的质量分数是多少?

酸、碱、盐在工农业生产、生活中应用广泛。请回答相关问题:
(1)硫酸是一种重要的酸,在稀释浓硫酸时 。盐酸、硫酸等酸具有相似的化学性质,是因为它们在水中都能够解离出酸根离子和H +,写出硫酸在水中解离的化学表达式 。
(2) 酸和碱的中和反应在实际中应用广泛。 我市某校化学实验室废液呈酸性, 应选用 试剂(指示剂)检验该废液。若直接排放会导致环境污染,从经济可行的角度考虑,选用 处理该废液。
(3)小苏打是焙制糕点所用的发酵粉的主要成分之一;在医疗上,它是治疗胃酸过多症的一种药剂,请写出该反应的化学方程式 。
(4)现有Ba(NO 3) 2溶液、稀硫酸、Na 2CO 3溶液、KOH溶液和CuSO 4溶液。 请从下列选项中选择能够与上述物质发生复分解反应、并有沉淀生成的物质。
A.稀盐酸 B.烧碱溶液 C.硝酸铵溶液
写出上述反应的化学方程式 。
现有下列实验装置,请根据学过的知识回答相关问题。

(1)写出实验仪器a的名称 。
(2)水是生命之源,自然界中的水都不是纯水,通过吸附、沉淀、过滤和蒸馏等方法可净化水,实验室和医疗上用的纯水,通常采用 方法制取。
(3)CO2用途较广,装置B可用于制取CO2.写出实验室制取二氧化碳的反应原理 ,实验室检验CO2气体的化学方程式 。
(4)B装置还可用于制取O2、H2等气体,写出实验室选择此装置制取氧气的化学方程式 ;如要收集较纯净的氢气可选用 装置。
(5)写出铁在氧气中燃烧的化学方程式 。