以饱和NaCl溶液和饱和NH4HCO3溶液为原料制备NaHCO3的原理为:NaCl+NH4HCO3═NaHCO3↓+NH4Cl.(已知NH4HCO3在40℃受热易分解)
回答下列问题:
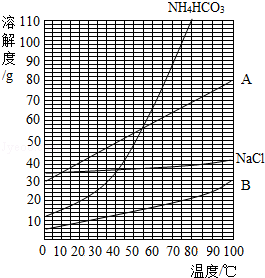
(1)该反应中的甲种物质溶解度曲线如图所示:
①35℃时,比较A、B溶解度的大小;A B.(填“<”或“>”).
②图中表示NaHCO3溶解度曲线的是 .(填“A”或“B”).
(2)为探究NaHCO3析出的最佳条件,完成了如图几组实验:
实验序号 |
反应温度/℃ |
反应时间/min |
NaHCO3产率/% |
a |
30 |
60 |
86.8 |
b |
30 |
120 |
X |
c |
35 |
60 |
89.4 |
d |
35 |
120 |
92.5 |
e |
40 |
60 |
85.3 |
f |
40 |
120 |
85.6 |
①实验c和d的目的是 .
②表格中X的数值可能为 .
A、85.8 B、86.8 C、92.1 D、93.1
③在相同反应时间,40℃时NaHCO3的产率比35℃时低的原因是 .
(每空2分,共8分)锶元素的粒子结构示意图和在元素周期表中显示的信息如图所示:
(1)锶属于__________元素(填“金属”或“非金属”)。
(2)锶元素的原子序数为__________,相对原子质量为______________________。
(3)图2所表示的粒子的化学符号是______________________。
(9分,每空1分)物质可根据其组成分为若干类,请把下表物质的种类补充完整,并仿照例子把下列物质:汽水、氮气、氯化钠、水、氧化铝、石灰石、铁丝、硫化氢按其所属类别填入相应空格:
| 物质类别 |
物质 |
|
| 混合物 |
例:空气、、 |
|
| 纯净物 |
例:Cu、(以下填化学式)、 |
|
| 化 合 物 |
例:NO2、、 |
|
| 非氧化物 |
例:NH4HCO3、 |
(7分,每空1分)用化学用语填空:
3个氢原子2个氧分子氮气
2个五氧化二磷分子2个亚铁离子
氢氧根离子3个硫酸根离子
某无色气体X可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或多种。为确认其组成,某同学取一定量该气体按下图所示装置进行实验(假设每步都充分反应或吸收),结果装置A中无明显变化,装置C增重1.8g,装置D增重2.2g。(提示:氢氧化钠固体有吸水性;)
(1)下列关于气体X成分的分析中,一定不含有;
可能含有的组成①;②;③;
(2)已知氢氧化钠与二氧化碳的反应类似于氢氧化钙与二氧化碳的反应,请写出氢氧化钠与二氧化碳的反应方程式;
实验是进行科学探究的重要方式,请根据下图回答问题: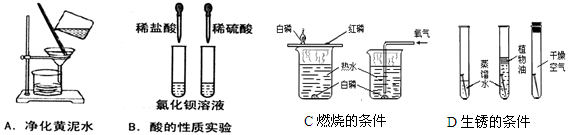
(1)用A图所示装置净化黄泥水时,玻璃棒的作用是___________________________。
(2)通过B图所示酸的性质实验,可认识到:虽然酸类物质具有相似的化学性质,但由于不同的酸溶于水时电离出的_________________不同,其性质也存在差异。
(3)实验C是通过控制哪些因素来探究可燃物燃烧的条件? 。
(4)请总结出铁制品发生锈蚀的主要条件? 。