结合下列实验装置,回答:
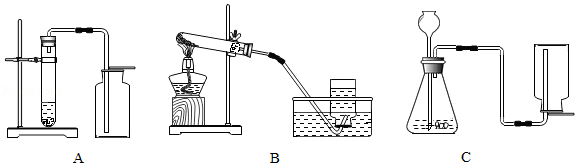
(1)实验室若用分解暗紫色固体制取O2,该固体的名称是 ,可选 (填字母,下同)装置。若用分解H2O2溶液制取O2,可选 装置。
(2)探究CO2性质的装置Ⅰ、Ⅱ如下:

①装装置Ⅰ,将Y形导管平放于桌面上,通入CO2后,观察到a管中试纸变红色,
b管中试纸无明显变化,此现象说明CO2能与 反应,生成的 使紫色石蕊变红色。
②装置Ⅱ,将Y形导管固定在铁架台上,a管在上方,b管在下方,通入CO2后,观察到b管中试纸先变红色且颜色较深,a管中试纸后变红色且颜色较浅,此现象说明CO2具有①所验证的性质外,还说明CO2的 。
(3)实验室制取CO2的化学方程式为 ,应选 (填字母)装置,选择该装置的理由是 。
在实验室里可采用多种方法制取氧气。
(1)写出用如图装置制氧气的化学方程式 。(写出一个即可)
(2)收集氧气可以采用排水法,这是利用了氧气的什么性质? 。

化学与人类社会生活密不可分,请回答下列问题。
(1)我们倡导“低碳”生活,“低碳”是指哪种物质的较低量排放? 。
(2)铝的化学性质活泼,为什么铝制品却有很好的抗腐蚀性能? 。
某小组用粗锌测定某稀硫酸中溶质的质量分数。取一定质量的稀硫酸于烧杯中,称量稀硫酸和烧杯的总质量;然后,向其中分两次加入粗锌(杂质不参加反应),实验过程和数据如图所示。请计算:

(1)生成氢气的总质量为 g。
(2)稀硫酸中溶质的质量分数。
湿法炼铜为我国首创。早在西汉时期,就有从胆矾水溶液中置换出铜的记载,其反应的化学方程式为:Fe+CuSO4═Cu+FeSO4.若采用此法炼制128t铜,需要消耗铁的质量是多少?
某兴趣小组发现某块土地玉米长势不好,为探究其原因,开启了项目学习之旅。
[查阅资料]玉米适宜在pH为6.0~7.0的土壤中生长;植物生长需要多种营养元素,包括碳、氢、氧、氮、磷、钾、钙、镁等大量元素和其他微量元素。
[任务一]检测土壤的酸碱度并制定改良方案
(1)检测该地土壤的酸碱度
可选用的实验用品:精密pH试纸(可精确到0.1)、标准比色卡、pH计、其他自选
|
实验步骤 |
测量结果 |
实验结论 |
|
步骤一:将3份不同位置的土样,干燥后分别与自来水按2:5的质量比在不同的烧杯中混合,充分搅拌后静置; |
试样一:pH=4.2 试样二:pH=4.4 试样三:pH=4.5 |
该土壤pH<6.0,不适合玉米生长 |
|
步骤二: 。 |
反思与评价:该实验方法有一处不够严密,请指出并说明原因 。
(2)探究熟石灰对土样酸碱性的改变情况
实验方法:取300g土样和 g蒸馏水混合,向其中加入一定量熟石灰,充分搅拌后静置,用pH计测定清液的pH;
测量结果:清液的pH为12.1;
反思:若要使改良的土壤适合玉米生长,需控制加入熟石灰的量。
(3)熟石灰用量的测定
实验目的:研究使300g土样呈中性所需的熟石灰的质量
实验方法: 。
(4)查阅资料,常用的酸性土壤改良剂有:生石灰、熟石灰、草木灰(主要成分K2CO3)、含钙的贝壳灰 (主要成分CaCO3) ; 要使改良后土壤的pH约为7,也可加入稍过量的 (从上述改良剂中选择)。
[任务二]分析土壤肥力
通过观察,该土地上玉米叶色略有发黄,且有倒伏现象;该小组同学建议施加适量含氮元素和钾元素的复合肥,如 。