某化学兴趣小组在学习酸碱中和反应实验时,进行了如下探究。
I.探究酸和碱能否发生反应
甲同学向盛有少量KOH溶液的试管中滴几滴无色酚酞试液,振荡,继续加入稀硫酸,观察到溶液由 色变成无色。甲同学得出结论:酸和碱能发生反应。
请写出稀硫酸和氢氧化钾溶液反应的化学方程式 。
Ⅱ.探究酸和碱反应后溶液中溶质的成分
乙同学对探究I中甲同学实验后的无色溶液展开探究
[提出问题]试管中无色溶液的溶质除了酚酞还有什么?
[提出猜想](1)K2SO4:(2)K2SO4和
[设计实验]
方案 |
实验操作 |
实验现象及方程式 |
实验结论 |
方案1 |
向试管中加入少量碳酸钠,然后加入过量甲同学实验后的无色溶液 |
可观察到溶液中有 气泡 产生。化学反应方程式为 。 |
猜想(2)成立 |
方案2 |
用玻璃棒蘸取少量反应后的溶液滴在pH试纸上 |
|
|
方案3 |
用玻璃棒蘸取少量甲同学实验后的无色溶液,然后慢慢加NaOH溶液,并不断振荡试管 |
无明显现象,过一会发现 . |
[发散思维]为了验证猜想(2)成立,你认为还可以选择的物质是 (填选项)。
A.Ba(NO3)2 B.锌粒 C.Cu D.盐酸
根据所学化学知识回答下列问题
(1)在粗盐提纯实验中,若蒸发时没有用玻璃棒搅拌,产率将会有什么变化
(2)小明在做过滤实验时,滤液流下速度慢的原因可能是什么?(答一点即可)
(3)木炭在氧气中燃烧时,木炭自上而下慢慢伸入到集气瓶底的目的是什么?
(4)做CO还原Fe2O3的实验时,为什么先通一会儿CO,然后再加热?
经过一年的学习,同学们认识了很多化学物质,它们在一定条件下可以转化或者相互反应。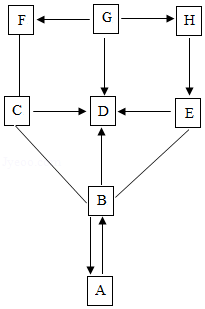
如图所示,A~H是初中化学所学的八种不同物质。“﹣”表示相连两物质之间能发生反应,“→”表示一种物质能转化成另一种物质。(部分反应物、生成物、反应条件已略去)
(1)已知A物质俗称纯碱,它的另一个俗称是 。
(2)已知H是磁铁矿的主要成分Fe3O4,F是黑色固体,则F是 O ,G→H的化学反应基本类型是 。
(3)D是 。
(4)写出B和C反应的化学方程式: 。
(5)写出A→B反应的化学方程式: 。
某班同学在实验室完成实验探究后得到废液A,其中含有稀硫酸、硫酸亚铁和硫酸铜。老师将同学们分成甲乙两组,继续进行如下实验,请完成下列相关问题:
[甲组任务]将废液转化成硫酸亚铁晶体。实验流程如图

(1)滤液B中的溶质来自于哪几个部分?
(2)写出上述流程中的一个化学反应方程式: 。
[乙组任务]利用废液来探究金属铝的化学性质。实验流程如图:
(3)滤渣C中一定没有 。
(4)滤液D中一定含有的溶质是 (填化学式,下同),可能含有的溶质是 。
生活中的泡沫灭火器常装有硫酸铝溶液和碳酸氢钠溶液,使用时把泡沫灭火器倒转,两种药液相互混合,发生如下化学反应:
1Al2(SO4)3+ NaHCO3═ Na2SO4+ Al(OH)3↓+ CO2↑
(1)请完成上述反应的化学方程式的配平。
(2)上述反应生成的大量二氧化碳跟发泡剂(主要成分是皂角等原料制取的液体)混合形成液体泡沫,从喷嘴中快速喷射出来,覆盖在燃烧物的表面,以达到灭火目的。其中应用的灭火原理有 。
(3)当电器发生火灾时,应先 ,然后才能使用泡沫灭火器。
(4)泡沫灭火器表面通常喷红漆防锈防锈的原理是 。
根据所学化学知识回答下列问题:
(1)我国古代画家用墨绘制的字画能够长时间保存的原因是什么?
(2)天气炎热时,鱼塘里的鱼为什么总是接近水面游动?