小红同学将未知浓度的过氧化氢溶液34g,加入盛有0.5g二氧化锰的烧杯中,待完全反应后,称得烧杯中剩余物质的质量为33.7g。计算该过氧化氢溶液中溶质的质量分数。
某工厂排出的废水中含有硫酸、硫酸铜,小艳同学取水样后进行研究性学习,请回答下列问题:
(1)小艳取少量废水于试管中,向其中加入氢氧化钠溶液,直至生成蓝色沉淀,写出生成蓝色沉淀的化学方程式: 。
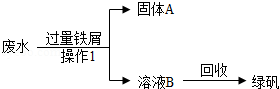
(2)如图是小艳记录的该工厂处理利用废水的简要流程:
操作Ⅰ的名称是 ,溶液B中的溶质是 。
化学课上,小亮与老师一起演示了如图所示的实验:

请回答下列问题:
(1)甲中铜加热时因生成了氧化铜而变黑,该变化属于 (填"物理"或"化学")变化.
(2)小亮将变黑的铜丝a伸入试管内的稀硫酸中,再取出时,铜丝表面又变红了,试管内发生反应的化学方程式是 ,该反应属于基本反应类型中的 反应.
(3)老师将加热变黑的铜丝b趁热迅速伸入试管内的活性炭中,再取出时,铜丝表面也变红了,则试管内活性炭的质量一定会 (填"增大"或"减小").
20℃时,将不同质量的NaCl晶体分别加入100g水中,充分溶解后所得溶液质量与加入NaCl晶体质量的对应关系如表:
|
组别 物质质量 |
A |
B |
C |
D |
E |
|
NaCl晶体质量/g |
5 |
15 |
20 |
30 |
40 |
|
所得溶液质量/g |
105 |
115 |
X |
130 |
136 |
请回答下列问题:
(1)A组的溶液为 (填"饱和"或"不饱和")溶液。
(2)C组X的值为 。
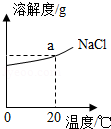
(3)如图为NaCl的溶解度曲线图,图上a点纵坐标的值为 。Ca(OH) 2的溶解度温度变化的趋势与NaCl相反,则室温时,向饱和石灰水加入少量生石灰,并恢复到室温,此时溶液中溶质的质量 (填">"、"<"或"=")原溶液中溶质的质量。
智能手机是一种多功能通讯工具,一款智能手机通常含有41种以上的化学元素,请回答:
(1)大部分手机外壳是用塑料或镁合金制成,二者中属于合成高分子材料的是
(2)手机线路的主要原料是铜,微电子材料还用到 金、银、钽等,在此主要利用了铜的 性.
(3) 手机屏幕大部分用的是硅酸铝玻璃 , 下列关于硅酸铝玻璃性质的推测不正确的是 (填序号)
①透光性好 ②常温下不易与氧气反应 ③易溶于水.
我国自主研制的首颗"碳卫星"将于2016年8月发射,主要任务是监测各地区二氧化碳的排放,为节能减排等宏观决策提供依据,请回答下列问题:
(1)大气中二氧化碳含量升高的一个主要原因是 燃料的大规模开发使用.
(2)固定和利用二氧化碳能有效减少空气中的温室气体.例如工业上利用CO 2和NH 3生产尿素的反应:CO 2+2NH 3  CO(NH 2) 2+X,则X的化学式为 .
CO(NH 2) 2+X,则X的化学式为 .
(3)下列行为符合"低碳生活,保护环境"这一理念的是 (填序号)
①焚烧纸质垃圾 ②步行上学 ③用电动牙刷刷牙.