实验室按如图步骤配制100g质量分数为22%的蔗糖溶液。
 回答下列问题:
回答下列问题:
(1)所需蔗糖的质量为 。
(2)用规格为 (填“50”、“100”或“500”)mL的量筒量取 mL蒸馏水倒入盛有蔗糖的烧杯中进行溶解。(水的密度约为1g/cm3)
(3)溶解时玻璃棒的作用是 。
(4)下列情况会导致所配溶液中溶质的质量分数偏高的是 (填字母序号)。
A.蔗糖中混有少量杂质
B.称量时蔗糖和砝码位置放反了(使用了游码)
C.用于溶解蔗糖的烧杯洗净后残留有少量的水
D.用量筒量取水时,俯视读数
某课外兴趣小组的同学对二氧化碳的制取和性质进行相关探究。
【实验回顾】
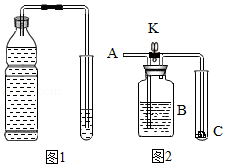
(1)实验室用大理石与稀盐酸制取二氧化碳的化学方程式为 。用向上排空气法收集二氧化碳的原因是 。
【实验探究】
(2)如图1所示,打开汽水瓶盖,有大量气泡冒出,塞上带导管的橡皮塞,导管另一端伸入装有滴加了紫色石蕊溶液的蒸馏水的试管中,轻轻振荡汽水瓶,观察到紫色石蕊溶液变红;加热上述试管,发现溶液颜色由红色变为紫色,写出上述变化过程中反应的化学方程式 , 。
(3)打开汽水瓶盖时,有大量气泡冒出,说明气体的溶解度随 。
(4)如图2所示,在C处放入用石蕊溶液染成紫色的干燥的纸花完成以下实验:
在A处持续而缓缓地通入气体X.当关闭K时,C处的紫色石蕊纸花不变色;当打开K后,C处的紫色石蕊纸花变为红色。
若气体X为未经干燥的二氧化碳,则B瓶中盛放的溶液可以为 (填字母)。
若气体X为未经干燥且混有氯化氢的二氧化碳,则B瓶中盛放的溶液可以为 (填字母)。
A.浓硫酸
B.氢氧化钠溶液
C.饱和碳酸氢钠溶液
【交流反思】
(5)该小组用空气样品和提高二氧化碳含量的空气的样品,控制相同条件测定二者在光照前后温度的变化,实验结果如图3.则与空气样品对应的温度变化曲线是 (填"a"或"b"),二氧化碳可以产生温室效应。
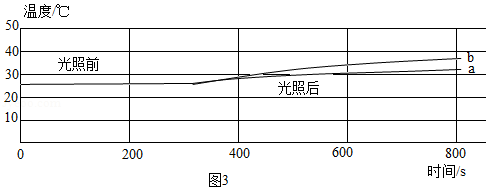
请简述温室效应对人类生存环境的功与过: (各写一点)。
化学兴趣小组的同学们在老师的带领下走进实验室,开展实验活动。
(1)实验室依次编号为1、2、3、4的药品柜中,分别存放常见的酸、碱、盐和酸碱指示剂。小刚欲使用熟石灰,他需从 号柜中取出。
(2)小刚发现盛放Na2CO3与NaCl两种溶液的试剂瓶标签脱落,为鉴别两种溶液,分别取样于试管中,加入无色酚酞溶液,若为Na2CO3,则观察到溶液变为 色。
(3)小文从柜中取出标有“10% NaOH溶液”的试剂瓶,取少量样品加入试管中,向其中滴入稀盐酸,发现产生气泡,判断该NaOH溶液中有Na2CO3,用化学方程式表示NaOH溶液变质的原因: 。
小文同学对变质的NaOH溶液进行如下一系列实验,实现药品再利用。
I.测定NaOH溶液中Na2CO3的质量分数
[实验操作]取40.0g 10%的NaOH溶液样品进行如图所示的实验。
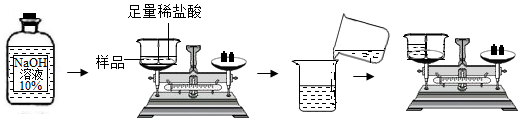
[数据处理]
①所取用盐酸(溶质质量分数7.3%)的质量理论上不少于 g。
②如图中,反应前后天平示数相差1.1g,计算NaOH溶液中Na2CO3的质量分数(写出计算过程)。
Ⅱ.变质的NaOH溶液再利用
小文将剩余NaOH溶液倒入烧杯中,加入经计算所需的熟石灰粉末,充分搅拌、静置,过滤,得到NaOH溶液和滤渣。充分搅拌的主要目的是 。
(4)实验结束后,同学们将实验产生的废液和废渣倒入指定的烧杯中,得到无色溶液和白色沉淀,溶液中除一定存在的溶质外,可能存在的溶质是 。
同学们再次实验,确认成分后,对废液回收利用,绿色排放。
U型玻璃管是常见的化学仪器,在实验中有广泛的应用。
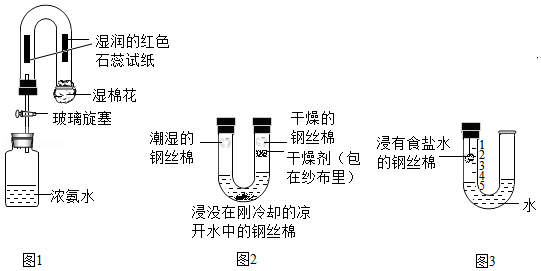
(1)借助U型玻璃管探究微粒的性质,如图1所示,打开玻璃旋塞,观察到湿润的红色石蕊试纸从左到右先后变蓝,该实验说明分子 ,湿棉花的作用是 。
(2)借助U型玻璃管探究钢铁锈蚀的条件,如图2所示:
①一段时间后潮湿的钢丝棉有明显锈迹,干燥的钢丝棉没有锈迹,此现象说明 。
②实验结束时,细心的同学发现浸没在凉开水中的钢丝棉也有少量锈迹,说明本实验有不完善之处,请利用原有装置提出具体改进方案 。
(3)借助U型玻璃管粗略测定空气中氧气的体积分数,如图3所示,得出空气中氧气体积分数约为五分之一的实验现象是 。
2019年春节起,常州大部分地区禁止燃放烟花爆竹,开启了龙城环保新时代。
(1)“禁止燃放烟花爆竹”的安全标志是 。

(2)禁止燃放烟花爆竹不仅可以减少噪声污染、火灾等,还以减少SO2和 等空气污染物的排放,提升空气质量。
(3)爆竹中常含有硫、硝酸钾和木炭的混合粉末,点燃后生成硫化钾(K2S)、氮气和二氧化碳,该反应的化学方程式为 。含硫燃料燃烧产生的SO2会形成 型酸雨,酸雨的pH (填序号)。
A.小于5.6 B.等于7 C.大于7
2019年1月,嫦娥四号和玉兔二号互拍成像,实现了探月工程五战五捷。
(1)嫦娥四号使用了大量复合材料。下列关于复合材料的说法中正确的是 。
A.不锈钢是常见的复合材料
B.复合材料集中了组成材料的优点
C.多种材料混在一起就是复合材料
(2)航天器的天线用钛合金制成。钛合金与金属钛相比, 的硬度更大。工业上通常是在高温下用四氯化钛(TiC14)与金属镁发生置换反应获得,该反应的化学方程式为 。
(3)航天器上的太阳能电池是将太阳能直接转化为 能的装置;大自然利用太阳能最成功的范例是 (填序号)。
A.火山爆发 B.温室效应 C.光合作用
