请根据下列实验图1回答问题。

(1)仪器a的名称是 。
(2)上述三个实验中,水对实验仪器起到安全保护作用的是 (填字母)。
(3)A实验中发生反应的化学方程式是 。
(4)对于B实验,小李同学进行了改进与创新,实验过程如图2所示:
如图2改进实验与B实验相比,明显的优点是 (写一条即可)。
“如何验证酸与碱反应生成水”是以下探究过程中的研究主题,请完成以下相关问题。
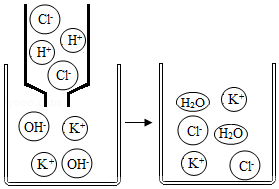
【知识回顾】实验证明酸与碱可发生中和反应,如图从微观角度说明中和反应的实质是 。
【提出问题】盐酸、硫酸等酸以酸溶液的形式存在,酸溶液与碱反应时,无法判断生成物中有“水”生成。如何设计实验验证酸与碱发生反应生成了“水”?
【查阅资料】冰醋酸即无水醋酸
蓝色硅胶遇水变红
【实验原理】CH3COOH+NaOH═CH3COONa+H2O,是冰醋酸与NaOH固体反应的化学方程式,CH3COONa在水溶液中可解离出自由移动的CH3COO﹣和Na+。
【进行实验】将适量的冰醋酸(CH3COOH)、NaOH固体及几粒蓝色硅胶置于试管中,塞上橡皮塞,轻轻振荡试管,观察到的现象是 。
【提出质疑】上述实验及实验现象,能说明“水”是化学反应生成的吗?该结论不严谨!
【解决方案】以科学严谨的态度思考,应在下列2个实验的基础上,再做上述实验。
|
实验方案(写出所用试剂即可)、实验现象 |
|
|
实验一 |
试剂与现象: 试 |
|
实验二 |
试剂与现象: |
【交流讨论】
(1)上述设计采用了 的实验方法。
(2)冰醋酸与NaOH固体充分混合后得到的固液混合物能够导电,是因为 。
教材中用图1实验来验证硫能在氧气燃烧,某化学兴趣小组对该实验进行了改进,改进后的实验装置如图2,请完成实验过程中的相关问题。

(1)根据图2进行实验,操作过程与现象记录如下:
①连接仪器,并在玻璃管中放入湿润的品红试纸及适量硫粉,向广口瓶中加入足量NaOH溶液。
②关闭止水夹,点燃酒精灯,加热,观察到硫粉熔化,并产生微弱的淡蓝色火焰。
③打开止水夹,通入氧气,观察到的现象:a. ,b.品红试纸褪色,c.小气球变大。
④硫粉完全反应后,熄灭酒精灯,继续通入氧气,排尽玻璃管中的SO2;待玻璃管冷却至室温时,关闭止水夹,撤下通入氧气的装置,然后应 ,并同时轻轻振荡广口瓶。
(2)问题讨论:
①图1实验设计中的不足之处是 。
②硫在氧气中燃烧更剧烈是因为 。
③反应过程中,玻璃管内湿润的品红试纸褪色,若改放干燥的品红试纸却不褪色,说明使品红试纸褪色的物质是 (提示:SO2与CO2的性质有相似之处)。
④广口瓶中吸收SO2的化学方程式为 。
实验室制取气体常用如图装置,请根据如图回答问题。

(1)写出图中标号仪器的名称:① 。
(2)实验室制取氢气的化学方程式为 ,若实验室用装置B制氢气,长颈漏斗的下端管口伸入液面下是为了防止 ,氢气的收集装置可选用 。氢气是一种高能燃料,点燃氢气前需要 。
(3)实验室将装置A和C组合,可制取的气体是 。
现有盛88.4g Na2CO3和NaOH混合溶液的大烧杯,向其中滴加质量分数为9.8%的H2SO4溶液,充分搅拌,烧杯中溶液的质量与滴加H2SO4溶液的质量关系如图所示,回答下列问题:
(1)写出AB段发生反应的化学方程式 。
(2)BC段可以观察到大烧杯的溶液中有气泡产生,则生成气体的质量为 g。
(3)B点时,大烧杯中的溶液pH 7(填“>”、“=”或“<”)。
(4)C点时,所得溶液为不饱和溶液。求溶液中溶质的质量分数。(写出计算过程)

将12.5g混有二氧化锰的氯酸钾固体加热至质量不再减少,冷却后称量固体的质量为7.7g。
(1)反应时生成氧气的质量为 g。
(2)计算反应前固体中二氧化锰的质量分数(要求写出计算过程)。