分析处理图表中的信息是学习化学的一种重要方法,如表是NH 4Cl和KNO 3在不同温度时的溶解度数据:
温度/℃ |
10 |
30 |
50 |
70 |
|
溶解度/g |
NH 4Cl |
33.3 |
41.4 |
50.4 |
55.2 |
KNO 3 |
20.9 |
45.8 |
85.5 |
110 |
|
根据上述数据,回答下列问题:
(1)从上表可知,50℃时,NH 4Cl的溶解度为 g.
(2)NH 4Cl和KNO 3的溶解度受温度影响比较大的物质是 (填化学式).
(3)欲配制质量分数为10%的KNO 3溶液,需要的玻璃仪器有烧杯、量筒、胶头滴管和 .
(4)烧杯中A中是60℃时,含有100g水的NH 4Cl不饱和溶液,经过如图1的变化过程
(在整个过程中,不考虑水分的蒸发),则C烧杯中溶液的质量为 g 
(5)某同学欲验证NH 4Cl固体溶于水时吸收热量,设计如图2实验,通过观察到 现象得以验证.
A.a端液面高于b端液面
B.a端液面低于b端液面.
化学是一门以实验为基础的科学,请结合下列装置图回答相关问题。

(1)仪器a的名称是 。
(2)实验室常用高锰酸钾制取氧气,其反应的化学方程式为 ,可选用的发生和收集装置是 (填字母编号)。
(3)实验室常用大理石和稀盐酸反应制取二氧化碳,其反应的化学方程式为 ,可以用E装置来收集,验满的方法是 。
(4)适合用D装置收集的气体必须具备的性质是 。
为探究酸、碱、盐的化学性质,某兴趣小組做了如下实验。

试回答下列问题
(1)试管A中的现象是 。
(2)试管B中反应的化学方程式为 。
(3)甲同学把反应后的C、D试管中的废液倒入一只洁净的烧杯中,观察到先有气泡产生,后有白色沉淀生成;过滤后得到白色沉淀和无色滤液。甲同学欲探究无色滤液中溶质的成分。
[提出问题]无色滤液中的溶质是什么?
[作出猜想]
猜想I NaCl
猜想I I NaCl和CaCl 2
猜想ⅢNaCl 和Na 2CO 3
猜想IV:NaCl、CaCl 2和Na 2CO 3
小明认为猜想IV定不成立,其原因是 (用化学方程式表示)。
[进行实验]
|
实验步骤 |
实验现象 |
实验结论 |
|
i.取少量滤液于试管中,滴加少量碳酸钠溶液 |
无明显现象 |
猜想 成立 |
|
ⅱ.取少量滤液于试管中,滴加少量 |
有气泡产生 |
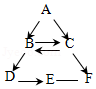
A一F为初中化学中常见的六种物质,其中B能供给呼吸,C是人体中含量最多的物质,D是黑色固体,E溶液呈蓝色,它们之间存在如图所示的转化关系(“一”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以转化为另一种物质,反应条件、部分反应物和生成物已略去)。
请回答下列问题:
(1)B生成D的反应属于 反应(填基本反应类型)。
(2)写出A→B反应的化学方程式 。
(3)写出C→F反应的化学方程式 。
某学习兴趣小组研究发现铜锈[Cu 2(OH) 2CO 3]在加热后,除有CO 2和水蒸气产生外,在试管的底部还有黑色的粉末生成,他们通过实验研究了黑色粉末的成分和所产生的气体。请填空。
(1)提出问题:黑色粉末是什么?
(2)猜想:黑色粉末可能是:
a.炭粉 b.氧化铜 c.
(3)查阅资料:炭粉和氧化铜均为黑色粉末,其中炭粉不与稀硫酸反应,也不溶于稀酸,而氧化铜可与稀酸反应而溶解。写出氧化铜和稀硫酸反应的化学方程式: 。
(4)设计实验方案:向试管中的黑色固体滴加足量的 (填"化学式")溶液,充分反应后,观察固体的溶解情况和所得溶液的颜色。
(5)现象与结论:
如果猜想a正确,则现象为 ;若现象是 ,则猜想b正确;假如现象为 ,则猜想c正确。
盐酸可以除铁锈。
(1)将一根生锈的铁钉放入足量的稀盐酸中,观察到铁锈逐渐消失,溶液由无色变成 ,该反应的化学方程式为 ,其基本反应类型为 。一段时间后,又观察到铁钉表面有气泡产生,该反应的化学方程式为 。
(2)写出一种防止铁制品锈蚀的方法 。