太阳能光伏发电最关键的材料是高纯硅。硅的原子结构简图为: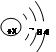
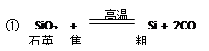 纯硅是通过以下过程制取的:(一)制粗硅:
纯硅是通过以下过程制取的:(一)制粗硅:
(二)制纯硅:② Si(粗)+ 2Cl2 SiCl4③ SiCl4 + 2H2
SiCl4③ SiCl4 + 2H2 Si(纯)+ 4HCl
Si(纯)+ 4HCl
纯净的无色透明的硅的氧化物(SiO2)晶体就是通常所说的水晶,这也许你不熟悉,但说起沙子,你一定不会陌生,沙子的主要成份即是SiO2,SiO2的化学性质与CO2有些类似。请根据以上信息,回答以下问题:
(1)X的值为。
(2)推断SiO2的物理性质(三点即可)、、。
(3)请写出SiO2与NaOH溶液反应的化学方程式:。
(4)在反应①②③中,②属于反应类型,属于置换反应的是(填序号)。
(5)化学上将只要有元素的化合价发生了变化的化学反应就叫做氧化还原反应,氧化还原反应中含有化合价升高了的元素的反应物叫还原剂,反应①中的还原剂是(写化学式)。
2011年3月11日,日本发生9.0级大地震,导致日本福岛第一核电站发生核辐射泄漏。
(1)福岛核电站机组反应堆芯发生核反应放出的氢气,接触外界的氧气发生剧烈反应,导致连续爆炸。请写出氢气爆炸时的化学方程式为。
(2)我国政府向日本提供了人道主义援助,援助的物质包括:一次性防护服,活性炭防护口罩,骨科内外固定材料,饮用水等等。其中防护口罩主要利用了活性炭的性。(3)由于堆芯熔毁,造成用来冷却反应堆的海水遭到反应堆内发生核裂变产生的放射性碘-131和铯-137的污染。由于运输困难和水资源遭到污染造成数百万人饮水困难。
① 生活中既能降低水的硬度,又能杀菌消毒的方法是_______________;
②“水是生命之源”。下列关于水的说法正确的是_______。
A.水是单质,能赋予生命
B.水是一种很好的溶剂,能维持人体的体液平衡
C.水资源紧缺既有缺水又有水受到污染的原因,所以既要节约用水又要防止水污染
D.水中氧元素含量很高,能提供人体所需的氧气
(4)这次因冷却故障导致核反应堆发生爆炸,为中国核电站的快速扩张和核安全敲响了警钟,应该思考如何和平、安全利用原子能。下列说法中正确的是。
A.核能的利用证实原子的可分性
B.核能的危害性太大,不应再推广使用
C.开发核能可节约化石能源
根据下面的溶解度表与溶解度曲线回答下列问题:
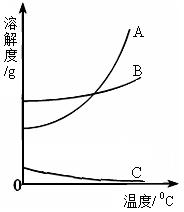
(1)B是______的溶解度曲线。
(2)40℃时,氯化钠的溶解度______(大于、小于或等于)硝酸钾的溶解度。
(3)硝酸钾中混有少量的氯化 钠,想要得到纯净的硝酸钾的方法是。
钠,想要得到纯净的硝酸钾的方法是。
(4)欲使硝酸钾的不饱和溶液转化为饱和溶液,可以采取的方法之一是。
(5)如图所示,烧杯A中是饱和的氢氧化钙溶液,向烧杯B中加入生石灰后,烧杯A中变浑浊,可能的原因是______(填序号)。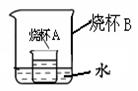
A.反应消耗水,氢氧化钙析出
B.反应放热,温度升高,氢氧化钙溶解度降低
C.生石灰与水反应生成的氢氧化钙不再溶解
有下列粒子:a.Fe3+ b.3H c.3N2 d.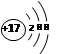 e.
e.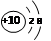
按要求填空:
(1)表示三个氮分子的是(填序号):。
(2)表示铁离子的是(填序号):。
(3)a与d两粒子结合形成物质的化学式是:。
(4)电工使用的试电笔触电发红光,是因为管内充气(名称)。
化学就在我们身边,与我们的生活息息相关。请回答以下生活中的问题:
(1)家用天然气(或液化气)中常添加一种具有特殊气味的物质乙硫醇。当闻到该气味时,提醒人注意天然气(或液化气)已经在泄露。能闻到乙硫醇的气味,这证实了分子________________的性质。
(2)“沙里淘金”说明黄金在自然界中能够以(填“单质”或“化合物”)形式存在。
(3)通常所说的煤气中毒是指由(填物质化学式)引起的中毒。
(4)长期使用的暖水瓶内胆常有一层水垢(主要成分为CaCO3、Mg(OH)2),可以用厨房中的调料除去。
(5)误食重金属盐(如:CuSO4、BaCl2等)可通过喝大量豆浆的方法解毒。你认为饮用下列物质也可以达到同样的目的(填字母)。
| A.牛奶 | B.果汁 | C.蛋清 | D.矿泉水 E、食盐水 |