Ca(OH)2变质得到Ca(OH)2和CaCO3的混合物。李琳同学设计了如图的实验装置来测定CaCO3的含量。她用气密性良好的装置装上药品并通一会儿N2后关闭止水夹,再打开分液漏斗活塞。提示:碱石灰(可以吸收CO2和H2O)、浓硫酸均足量,稀盐酸不考虑其挥发性。
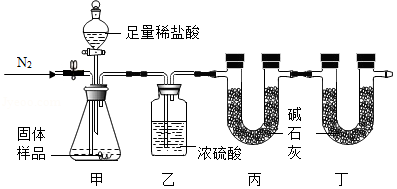
(1)通入N2的原因之一是N2的化学性质 (填“活泼”或“不活泼”)。
(2)甲装置中发生中和反应的化学方程式为 。
(3)浓硫酸的作用是 。
(4)测定CaCO3的含量需要测定两个物理量,其中一个物理量为样品的质量。
①另一个物理量为 (填序号)。
A.滴下的稀盐酸质量
B.反应前后乙装置增加的质量
C.反应前后丙装置增加的质量
D.反应前后丁装置增加的质量
②若去掉丁装置,测得CaCO3含量 (填“偏高”、“偏低”或“不变”)。
③甲装置中反应结束后打开止水夹再通入一会儿N2的目的是 。
“84消毒液”是一种常用含氯消毒用品,有效成分是次氯酸钠(NaClO)。使用时,可根据实际需求进行配比,并规范使用,以防引发危险。
(1)“84消毒液”中的有效氯来自次氯酸钠,计算次氯酸钠中氯元素的质量分数。(计算结果精确到0.1%)
(2)现需要5L有效氯浓度为500mg/L的稀溶液,选用有效氯浓度为50000mg/L的某品牌“84消毒液”进行配制,需加水多少升?( 忽略混合前后溶液体积的变化)
(3)“84消毒液”不能与洁厕灵混合使用,因为“84消毒液”里的次氯酸钠与洁厕灵里的盐酸会发生化学反应,产生的氯气对人体有害,不同浓度氯气对人体的影响如表所示。
|
浓度(mg/m3) |
对人体的影响 |
|
3000 |
可立即麻痹呼吸中枢,导致瞬间死亡 |
|
120﹣170 |
极为危险,会引起急性肺水肿及肺炎 |
|
40﹣60 |
在1小时内便可致人严重中毒 |
通过计算分析,在10米3密闭空间里,若将1.49克次氯酸钠与盐酸完全反应,产生的氯气会对人体造成怎样的影响?(次氯酸钠与盐酸反应的化学方程式为:NaClO+2HCl═NaCl+Cl2↑+H2O)
随着手机、电脑等移动设备的普及,人们对充电设备的要求越来越高。最近,某品牌氮化镓充电设备以体积小、功率大深受消费者喜爱。
(1)氮化镓(GaN)是充电设备中的核心材料。查阅资料得知:氮化镓中氮元素的化合价与氨气(NH3)中氮元素的化合价相同。由此可知,氮化镓中镓元素的化合价为 。
(2)氮化镓的制取可通过镓与氨气在高温下发生置换反应来实现,其反应的化学方程式为 。
工业纯碱中含少量氯化钠。兴趣小组分别采用不同的方法测定工业纯碱样品中碳酸钠的质量分数。
(1)方法一:差量法。称取W克样品与足量的稀盐酸充分反应,生成的二氧化碳通过装有试剂X的乙装置,并利用测量乙装置增加的质量,求得样品中碳酸钠的质量分数。该方法中试剂X可选用 。
(2)方法二:沉淀法。称取15克样品完全溶解于水中配成60克样品溶液,取三个烧杯分三次进行实验,每次加入30克氯化钙溶液充分反应,过滤、洗涤、干燥所得的沉淀质量记录如表。计算样品中碳酸钠的质量分数。
(Na2CO3+CaCl2═CaCO3↓+2NaCl)
|
烧杯1 |
烧杯2 |
烧杯3 |
|
|
样品溶液(克) |
10 |
20 |
30 |
|
氯化钙溶液(克) |
30 |
30 |
30 |
|
沉淀质量(克) |
2 |
4 |
5 |
(3)请写出提高方法一测量精确度的操作建议(写出2条) 。

小明利用稀硫酸与生锈的铁屑反应制取硫酸亚铁,实验流程如图:

资料:①Fe2(SO4)3+Fe═3FeSO4;②硫酸亚铁容易被氧化为硫酸铁等物质。
(1)配制50克溶质质量分数为19.6%的稀硫酸,需溶质质量分数为98%的浓硫酸 克。
(2)写出该实验中的一条化学方程式(除资料①中的反应外) 。
(3)稀硫酸与生锈的铁屑充分反应后,要确保铁有少量剩余,其目的是 。
新冠疫情发生以来,在“坚定信心、同舟共济、科学防治、精准施策”的思想指引下,中国抗疫取得重大胜利!
(1)对新型冠状病毒的毒株分离和基因测序,是研发疫苗和药物的基础。为应对疫情,同学们都居家学习,在此期间做法合理的有 。
A.健康饮食,平衡膳食
B.长时间躺床上看书
C.多服用抗生素增强抵抗力
D.关爱家人,乐观面对生活
(2)佩戴口罩出行是预防新冠肺炎的重要举措。一次性口罩需要及时更换,废弃的口罩应放入 垃圾桶最合适。
(3)对公共场所的定期消毒是控制新冠肺炎的有力保障。“84”消毒液被广泛用于新冠疫情的卫生消毒,可通过氯气与氢氧化钠反应制取,生成物中有氯化钠、次氯酸钠(NaClO) 和水,其中次氯酸钠是消毒液的有效成分。
①次氯酸钠中氯元素的化合价为 。
②写出制取“84”消毒液的化学方程式 。
