“84消毒液”是一种常用含氯消毒用品,有效成分是次氯酸钠(NaClO)。使用时,可根据实际需求进行配比,并规范使用,以防引发危险。
(1)“84消毒液”中的有效氯来自次氯酸钠,计算次氯酸钠中氯元素的质量分数。(计算结果精确到0.1%)
(2)现需要5L有效氯浓度为500mg/L的稀溶液,选用有效氯浓度为50000mg/L的某品牌“84消毒液”进行配制,需加水多少升?( 忽略混合前后溶液体积的变化)
(3)“84消毒液”不能与洁厕灵混合使用,因为“84消毒液”里的次氯酸钠与洁厕灵里的盐酸会发生化学反应,产生的氯气对人体有害,不同浓度氯气对人体的影响如表所示。
浓度(mg/m3) |
对人体的影响 |
3000 |
可立即麻痹呼吸中枢,导致瞬间死亡 |
120﹣170 |
极为危险,会引起急性肺水肿及肺炎 |
40﹣60 |
在1小时内便可致人严重中毒 |
通过计算分析,在10米3密闭空间里,若将1.49克次氯酸钠与盐酸完全反应,产生的氯气会对人体造成怎样的影响?(次氯酸钠与盐酸反应的化学方程式为:NaClO+2HCl═NaCl+Cl2↑+H2O)
将含有NaCl杂质的某烧碱样品10g完全溶于90g水中,再向所得溶液中慢慢滴入溶质质量分数为7.3%的稀盐酸.在实验过程中,溶液的pH与滴入稀盐酸的质量关系如图所示.
(1)求l0g该样品中氢氧化钠的质量.
(2)求a点时,溶液中溶质的质量分数(计箅结果精确到0.1%)

青少年过多摄人蛋糕里的人造奶油会产生一种影响身体发育的反式脂肪酸,其化学式为C 18H 34O 2,请计算。
(1)该反式脂肪酸中碳、氧元素的质量比 。
(2)141g该反式脂肪酸中含氢元素的质量为 g。
学校实验室的废液缸中收集了学生在实验室制取CO 2后残留废液.某化学课外小组的同学想探究废液中溶质的成分,请我们共同参与探究并回答下列问题:
【提出问题】废液中的溶质是什么物质?
【作出猜想】甲同学认为废液中的溶质只有CaCl 2.你认为还可能含有的溶质是 (化学式).
【査阅资料】CaCl 2溶液呈中性.
【实验与结论】①甲同学取少量CaCl 2溶液和废液分别加入到2支试管中,并向其中分别滴加无色酚酞试液做对比实验,结果两试管中溶液均无色,于是甲同学认为自己的猜想是正确的.
②你认为甲同学的实验 (填"能"或"不能")证明他的猜想,理由是 .
③如果要证明你的猜想是正确的,你选择的试剂是 ,实验中可能观察到的现象是 .
【拓展与应用】①若实验证明你的猜想是正确的,想要处理废液只得到CaCl 2溶液,应向废液中加入过量的 ,反应完全后过滤.
②通过以上探究,你认为实验室的废液未经处理直接倒入下水道,可能造成的危害是 .
根据如图回答问题:
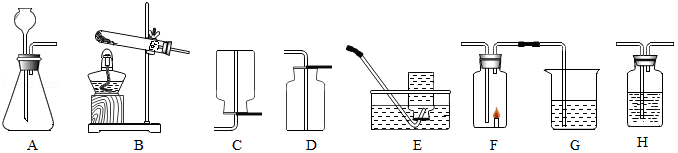
(1)实验室用高锰酸钾制取氧气的发生装置是 (填装置字母序号),该反应的化学方程式为 。
(2)选择气体收集方法时,必须考虑的气体性质有 (填序号)。
①颜色 ②密度和溶解性③可燃性
(3)某同学连接A、F、G进行实验,A中所加药品不同,G中所加药品相同,为Ca(OH) 2溶液。
①若实验时F中蜡烛熄灭,G中溶液变浑浊,则A中反应的化学方程式为 。
②若实验时F中蜡烛燃烧更旺,则A中产生的气体是 ,还需将气体通过盛有 (填药品名称)的洗气瓶H。
③若将G中的白色浑浊物从液体中分离出来的操作名称是 。
为了节约林木资源,近几年兴起了一种含碳酸钙的“石头纸”,这种“石头纸”是用沿海水产养殖中大量废弃贝壳制得的,为测定其中碳酸钙(杂质不溶于水也不与水反应)的含量。某校化学兴趣小组的同学进行了如下实验(水和氯化氢的挥发忽略不计);取25.0g样品粉碎放入烧杯中,加入一定质量分数的稀盐酸,所加稀盐酸的质量与生成气体的所量关系如图所示:
(1)计算“石头纸”中碳酸钙的质量分数。
(2)完全反应后烧杯内溶液的溶质的质量分数是多少?(结果精确到0.1%)
