某同学利用“氢气还原氧化铜的实验”测定水的组成。回答下列问题:
(1)用锌粒和稀硫酸反应制取氢气。反应的化学方程式为 ;从下列装置中选择并组装一套可以“随时控制反应的发生与停止”的装置,制取并收集干燥的氢气,正确的连接顺序为 (填接口处字母标号);仪器①的名称是 。

(2)利用如图装置测定水的组成(尾气处理装置及H2验纯等操作均未列出)
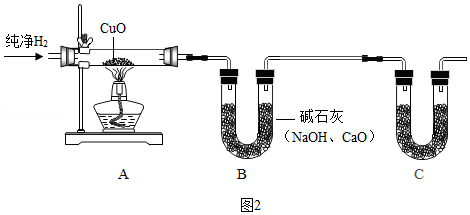
①下列操作的正确顺序为 (填字母序号)。
a.点燃酒精灯 b.通入H2 c.停止通入H2 d.熄灭酒精灯
②装置C的作用是 。
(3)若装置A中的玻璃管和其中的物质在反应前后的质量差为m1,装置B和其中的物质在反应前后的质量差为m2,则水中H、O元素的质量比为 (用含m1、m2的代数式表示)。
如图是初中化学课本中的部分实验。请回答下列问题: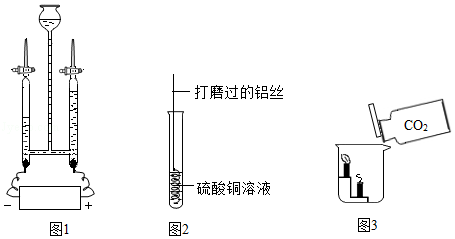
(1)图1电解水实验证明水是由 组成的。
(2)写出图2反应的化学方程式: 。
(3)图3阶梯蜡烛实验得出有关二氧化碳的化学性质: 。
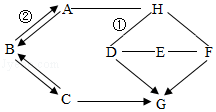
A~H是初中化学常见的8种不同物质,其中D为铁锈的主要成分,A~G均含有同一种元素,F广泛应用于造纸制玻璃及印染工业,H中只含有两种元素。A、B、C、E、F为五种不同类别物质,反应②放热。它们之间的转化和反应关系如图所示,图中“→”表示一种物质转化为另一种物质,“﹣”表示相连的两种物质能发生化学反应,部分反应物、生成物及反应条件已略去。请回答:
(1)E所属物质类别是 (填“单质”、“氧化物”、“酸”、“碱”或“盐”)。
(2)G的化学式 。
(3)物质A在生产生活中的用途 (答出一点即可)。
(4)写出反应①②的化学方程式:
① :② 。
化学来源于生活,通过学习化学,你会发现化学就在身边。用化学知识可以解释生活中的一些事例和现象。
(1)回收废旧金属的好处: (答出一点即可)。
(2)湿衣服在阳光下比在阴凉处干得更快 。
(3)篝火晚会结束时,用水将篝火浇灭,原理是 。
(4)口服含“氢氧化铝”的药物治疗胃酸过多: (用化学方程式表示)。
2019年6月6日中国女排获得世界女排联赛香港站冠军。
(1)牛肉炖西红柿是很多女排运动员比较喜爱的一道美食,其中西红柿中富含的营养素(除水外)是 。
(2)大米是水稻磨制而成的。在水稻种植过程中离不开施肥,NH4NO3是农业上常用的 (填“氮”、“钾”或“磷”)肥,但不能跟碱性物质混合使用,原因是 。
(3)女排运动员使用的下列物品中属于合成材料的是 (填字母序号)
A.玻璃水杯
B.纯棉毛巾
C.手机塑料外壳
将12.5g石灰石(杂质不与酸反应也不溶于水),加入到装有100g稀盐酸的烧杯中。恰好完全反应后,烧杯中物质的总质量为108.1g。请计算。
(1)生成二氧化碳的质量为 g。
(2)求稀盐酸中溶质的质量分数(写出计算过程)。