小苏打和食盐是厨房中常见物质。现有一包白色固体,可能由碳酸氢钠、氯化钠中的一种或两种物质组成。某科学小组同学展开了系列研究。
(一)定性分析
[实验目的]确定白色固体的组成
[实验方案]:如图1所示:
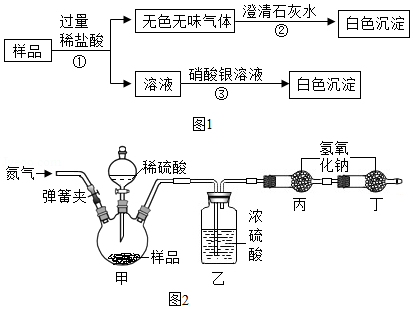
[实验结论]小明同学经过上述实验得出结论:该白色固体由碳酸氢钠、氯化钠两种物质组成。
(1)步骤①发生反应的化学方程式是 ;
(2)步骤②中的澄清石灰水也可以用其它碱溶液代替,如 ;
(3)科学小组认真研究讨论后认为,此方案不能得出小明同学的结论。一致认为将上述方案中使用的一种试剂进行调换,如仍出现上述现象,则小明同学的结论正确。调换措施是 。
(二)定量分析
[实验目的]测定该白色固体中碳酸氢钠的质量分数
[实验方案]该小组利用图2所示的实验装置(固定装置已略去,装置气密性良好)进行实验,每一步反应均完全进行。
(1)首先称取a克该样品放入装置甲中,然后进行有关实验操作,正确的顺序是 (填序号,可重复选择)
a.称量装置丙的质量
b.打开弹簧夹,通入足量的氮气,关闭弹簧夹
c.打开分液漏斗的活塞,注入足量的稀硫酸,关闭活塞
(2)如果没有装置乙,会造成测定结果 (填“偏大”“偏小”或“不变”);
(3)装置丁的作用是 。
(三)拓展交流
经査阅材料:将二氧化碳气体持续通入一定量的氢氧化钠溶液中会先后发生以下两个化学反应:
①2NaOH+CO2=Na2CO3+H2O ②Na2CO3+CO2+H2O=2NaHCO3
小明同学将5g二氧化碳气体通入100g 5%的氢氧化钠溶液中,充分反应后,所得溶液的溶质是
(填化学式)。
维生素C主要存在于蔬菜、水果中,其分子式为C 6H 8O 6,在空气中易氧化变质.
(1)维生素C中C、H、O三种元素的质量比为 (用最简比表示).
(2)为测定某鲜榨橙汁中维生素C的含量,兴趣小组进行如下实验:
步骤1 取橙汁样品,加入活性炭,振荡、静置、过滤,滤液移至小烧杯中,盖上玻
璃片.
步骤2 配制碘(I 2)溶液,测得其浓度为1.27g/L(即1升碘溶液中含有1.27克I 2).
步骤3 快速移取20.00mL处理后的橙汁样品置于锥形瓶中,滴入碘溶液,恰好完全反应时消耗碘溶液10.00mL.(测定原理:C 6H 8O 6+I 2═C 6H 6O 6+2HI)
①步骤1中活性炭的作用是 .
②步骤3必须在步骤1、步骤2之后立即进行的原因是 .
③计算1L该橙汁样品中含有维生素C的质量: g.(请写出计算过程)
神舟十一号与天宫二号的成功对接增强了国人的民族自信,推动了相关领域的研究.
(1)合金材料的研发
①合金的很多性能与组成它们的纯金属不同.图1能表示锡铅合金的是 (填序号"a""b"或"c").
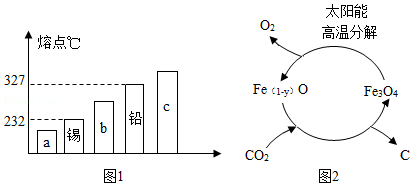
②镁合金被誉为"21世纪绿色金属结构材料".Mg 17Al 12是一种特殊的镁合金,通常选择真空熔炼而非空气中熔炼的原因是 (任写一个化学方程式).该合金是一种储氢材料,完全吸氢后得到MgH 2和Al,"储氢过程"属于 (填"物理"或"化学")变化.
(2)合成材料的改良
①碱式碳酸铝镁[Mg aAl b[OH] c(CO 3) d•χH 2O]是一种新型塑料阻燃剂,其中a、b、c、d的代数关系式:2a+3b= .
②大部分塑料在自然环境中很难降解而造成"白色污染",为缓解这一环境问题可采取的措施有 (答出一点即可).
(3)CO 2的绿色利用
①目前空间站处理CO 2的一种方法是在催化剂作用下,利用H 2使CO 2转化为甲烷并得到生活用水.该反应的化学方程式为 .
②以"铁氧化物"为催化剂,利用太阳能将CO 2热解为碳和氧气,这一转化过程(如图2)中化合价升高的非金属元素是 .
空气中氧气含量测定的经典赏析。
教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图)。

(1)写出汞与氧气反应的化学方程式 。
(2)本实验中选择使用汞的优点有:
①汞在加热的条件下,只和氧气反应。②汞为液态,在汞槽中起到液封的作用,并能直接用来测见反应器内空间体积的变化。
③生成的氧化汞分解又能得到汞和氧气,把得到的氧气加到剩下的  体积的气体中,结果所得气体跟空气的性质完全一样。
体积的气体中,结果所得气体跟空气的性质完全一样。
根据资料卡片,请再补充本实验使用汞的两个优点,并说明依据。
④ 。 ⑤ 。
(3)通过实验,拉瓦锡得出了空气由氧气和氮气组成,其中氧气约占空气总体积  的结论。请根据现在的认识,对此结论予以补充。 。
的结论。请根据现在的认识,对此结论予以补充。 。
核电荷数为1~18的元素的原子结构示意图等信息如下,请回答下列问题。

(1)2017年5月9日,中国科学院等单位联合发布了115号元素的中文名为"镆"。此元素原子的核电荷数为 ,核外电子数为 。
(2)在第三周期中,随着原子序数的递增,元素原子核外电子排布的变化规律是 。
(3)利用上表中给出的元素,写出含有氮元素的常见单质、氧化物、酸、碱、盐的化学式各一个,并标出所写化学式中氮元素的化合价:单质 、氧化物 、酸 、碱 、盐 。
(4)以钠和氯为例,简述结构与性质的关系。 。
(5)国产C919大型客机上使用了大量的铝合金。工业上用电解氧化铝(Al 2O 3)得到铝和氧气、试计算电解102t氧化铝最多能生成铝的质量是多少?(写出计算过程)
溶液在生产、生活中起着十分重要的作用。请回答下列问题:
(1)可以作为溶质的是 。
A.只有固体 B.只有液体 C.只有气体 D.气体、液体、固体都可以
(2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为 ,水的体积为 mL (水的密度近似看作1g/cm 3)。
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如图1.t 1℃时,甲物质的溶解度是 。t 2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是 (填"甲"或"乙")物质的饱和溶液。
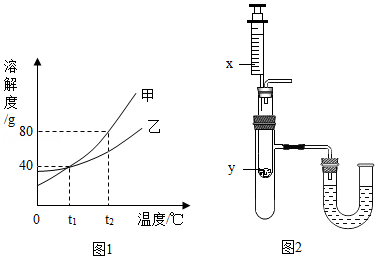
(4)按图2所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液面升高。则可能的组合是 。
|
选项 |
x |
y |
|
A |
水 |
氧化钙 |
|
B |
水 |
硝酸铵 |
|
C |
浓硫酸 |
水 |
|
D |
稀盐酸 |
镁 |