工业上采用离子交换膜电解槽电解饱和食盐水,可得到高浓度的烧碱溶液(含NaOH 35%~48%),某兴趣小组欲验证一化工厂生产的NaOH溶液是否达到了高浓度标准,进行了如下操作,请你参与计算:
(1)用37%的浓盐酸配制200g7.3%的盐酸,需要加水(密度为1g•mL﹣1) mL.(计算结果保留一位小数)
(2)采集该化工厂电解槽中的NaOH溶液20g,向其中滴入所配制的盐酸,当溶液的pH=7时,消耗盐酸100g,判断电解槽中NaOH溶液是否达到高浓度标准。(写出计算过程)
用煤直接做燃料如果不进行处理,会因煤中的硫生成SO2气体造成大气污染。
(1)现有南方产的一种煤含硫8%.某火力发电厂燃烧100t这种煤,假设燃烧时煤中的硫全部转化为SO2,则产生SO2的质量是多少?
(2)如在煤中混入粉末状的石灰石,则燃烧产生的SO2会与CaCO3反应生成CaSO3进入炉渣而减少大气污染。取50g此炉渣(含24%CaSO3)逐滴加入20%的盐酸,请在如图坐标中画出相应的曲线图(纵坐标为盐的质量,请设定具体物质;并标出曲线中必要的数据)。
[已知]①设炉渣已不含石灰石,炉渣其它成分不与盐酸反应;
②CaSO3和盐酸反应类似于CaCO3。
(3)向燃烧后的烟气喷洒石灰浆也可吸收SO2生成CaSO3.现用一万元分别购买两种原料来除去SO2,相关数据如表:
|
方法 |
物质 |
相对分子质量 |
纯度 |
价格(元/t) |
除SO2的量(t) |
|
A |
石灰石 |
100 |
90% |
200 |
14.4 |
|
B |
熟石灰 |
74 |
94% |
500 |
14.6 |
方法B比方法A除SO2的量略大,而且工业上多数采用方法B.其原因分别是: 。
大型电动车使用的磷酸亚铁锂(LiFePO4)电池,具有“体积小、成本低、充电快、输出功率高、循环寿命长”等优点。回答问题:
(1)磷酸亚铁锂中非金属元素的原子个数比为 。
(2)磷酸亚铁锂中锂、磷元素的质量比为 。
(3)磷酸亚铁锂中铁元素的质量分数为 (精确到0.1%)。
请参与下列探究实验:
[实验探究]
|
步骤 |
实验操作 |
实验现象 |
结论或解释 |
|
(1) |
用玻棒分别蘸取95%的酒精、蒸馏水置于火焰上。 |
酒精 , 蒸馏水 。 |
结论:酒精是可燃物,水不是可燃物。 |
|
( 2) |
在铁片两端放大小相同的硬纸片、乒乓球碎片,在铁片中间加热。 |
乒乓球碎片先燃烧、硬纸片后燃烧。 |
结论:乒乓球碎片的 比硬纸片的低。 |
|
(3) |
在如图中打开分液漏斗的旋塞。
|
①溶液中产生气泡; ②蜡烛火焰a (填"先于""后于") b熄灭。 |
现象②的原因是:CO 2不助燃; 。 |
|
(4 ) |
用大烧杯罩住高低两支点燃的蜡烛。
|
①烧杯底部变黑; ②蜡烛火焰d比c先熄灭。 |
CO 2不助燃,蜡烛不完全燃烧;d先熄灭的原因是: 。 |
[拓展]堆积的面粉不容易点燃,即使少量点燃也只是小火燃烧;如果把面粉撒向空中遇火星可能会发生爆炸。"小火燃烧"和"发生爆炸"的原因分别是: 。
根据如图(省略夹持仪器)回答问题:
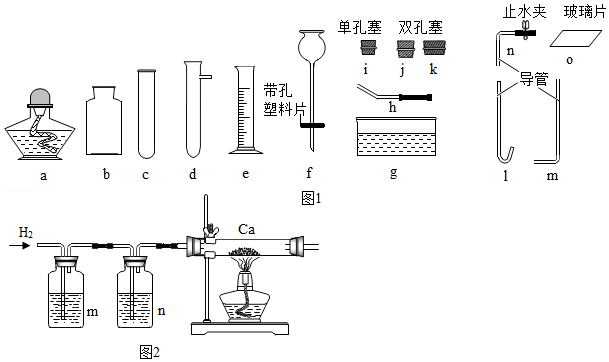
(1)仪器e的名称是 。
(2)用高锰酸钾分解制取氧气的化学方程式为 ,制备并导出氧气的装置应选取的仪器是c、h、 (填序号),收集氧气(用于做铁丝燃烧实验)应选取的仪器是 (填序号)。
(3)用锌粒和稀盐酸制备H2 (可随时使反应发生或终止)应选取的仪器是 (填序号)。
(4)氢化钙(CaH2)常温下能与水反应生成H2,是野外工作人员便携燃料的来源。课外小组同学利用(3)中产生的H2与金属钙反应制取CaH2 (见图2)。请回答:
①洗气瓶中m、n应选下列试剂的 、 (填序号);
I.NaHCO3溶液、Ⅱ、NaOH溶液、Ⅲ.浓硫酸。
②为防止钙被氧化,在加热钙之前必须进行的操作是 。
③CaH2与水反应的化学方程式为 ;为防止空气中的O2、CO2水蒸气与玻璃管中Ca或CaH2反应,必须在导管末端再连接的装置是(说出仪器名称及所装试剂) 。
孔雀石主要成分为Cu2(OH)2CO3 (难溶于水),还含有少量SiO2(难溶于水、不与稀硫酸反应)、Fe2O3等杂质。现以孔雀石为原料制取胆矾(CuSO4•5H2O)的部分工艺流程如图。

请回答:
(1)滤渣b的化学式为 。
(2)溶液c中的溶质有(写化学式):H2SO4、 、 。
(3)盐溶液d的颜色为 ;实验室蒸发溶液时用到的玻璃仪器有 (写1种)
(4)在气体a生成CaCO3的过程中,发生反应:CO2+CaCl2+2NH3+H2O=CaCO3↓+2X,X的名称为 ;孔雀石与稀硫酸反应生成气体a的化学方程式为 。