如图为某些物质间的转化关系,甲、乙、丙均为气体,乙有激性气味,丁是应用最广泛的金属。A是大理石的主要成分,G是一种化肥,H为红棕色固体。部分反应物和生成物已略去。

(1)化学式:B ,F 。
(2)自然界中,甲和D反应产生一种供给呼吸的气体,该反应名称为 。
(3)反应①、②的化学方程式:① ;② 。
(4)由反应②可知,在农业上施用G时应注意 。
根据下列实验装置图;回答问题。

(1)写出标号a仪器的名称 。
(2)实验室用氯酸钾和二氧化锰混合加热制取氧气,发生装置应选 (填字母,下同);写出过氧化氢溶液和二氧化锰混合制取氧气的化学方程式 。
(3)实验室用石灰石和稀盐酸制取二氧化碳气体所选装置为 ;若要检验该气体,应在F中加入的试剂为 。
研究小组对氯水(氯气的水溶液)进行探究.
(1)测定氯水的酸性:取少量,向其中滴加(选填指示字母) ,一开始应观察到滴加的指示剂在氯水中 色.
a.无色酚酞试液 b.紫色石蕊试液
(2)氯水具有漂白性,请你参与"氯水使品红试纸褪色"的研究.
【提出问题】氯水中的什么成分使品红试纸褪色?
【猜想】
猜想1:氯水中的水使品红试纸褪色.
猜想2:氯水中的Cl 2使品红试纸褪色.
猜想3:氯水中的HCl使品红试纸褪色.
猜想4:氯水中的 (填化学式)使品红试纸褪色.
【实验探究】
|
实验操作 |
实验现象 |
结论 |
|
①用水润湿品红试纸,观察 |
|
猜想1不成立 |
|
②把品红试纸放入干燥的氯气中,观察 |
试纸不褪色 |
猜想2不成立 |
|
③ ,观察 |
试纸不褪色 |
猜想3不成立 |
【结论】通过探究,找到了氯水中使水使品红试纸褪色的原因.
【思考】实验(1)向氯水中滴加几滴所选指示剂后,最终观察到的现象是 .
实验室制备氯气通常用浓盐酸与MnO2反应制得:
4HCl(浓)+MnO2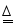 Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O
用下列实验室常用装置或仪器(铁架台、夹持和连接装置略)的字母填空.

(1)制氯气需要的装置和仪器是 .
(2)实验室进行氯气制取或性质试验后,必须用G装置进行尾气处理,防止污染空气.说明氯气具有 性.
(3)收集氯气的装置是 ;干燥氯气可用装置 .
为探究一瓶久置的氢氧化钠溶液(原溶质质量分数16%)是否变质,同学们提出了多种方案,其中一种方案设计如下:
【查阅资料】:氢氧化钠溶液与空气接触可能发生的反应:
2NaOH+CO 2═Na 2CO 3+H 2O
Na 2CO 3+CO 2+H 2O═2NaHCO 3
NaOH与NaHCO 3在溶液中发生反应:
NaOH+NaHCO 3═Na 2CO 3+H 2O
【假设猜想】:1.该溶液未变质,溶质成分只有NaOH
2.该溶液已变质,…
【实验探究】:向一定质量的洁净烧杯中加入m 1g该氢氧化钠溶液,再加入溶质质量分数为20%硫酸m 2g(硫酸 足量),充分反应、冷却后称量.根据溶液总质量m判断该氢氧化钠溶液是否变质.
试结合该方案,回答下列问题:
(1)进行上述实验使用的称量仪器名称是 ,称量时,烧杯应放在该仪器的 盘.
(2)实验探究中,烧杯内溶液总质量m与氢氧化钠溶液是否变质的对应关系是:
m<(m 1+m 2)g,猜想 成立;m=(m 1+m 2)g,猜想 成立.
(3)补充完善猜想2:如果该溶液部分变质,溶质的成分为 (填化学式,下同);
如果该溶液完全变质,溶质成分可能为Na 2CO 3或NaHCO 3或 .
某化学兴趣小组把金属钠放到硫酸铜溶液中,实验并非如想象的有红色铜析出,而是生成一种蓝色沉淀,同学们非常好奇进行实验探究.
(1)【提出问题】金属钠放到硫酸铜溶液中到底发生了怎样的化学反应?
(2)【查阅资料】钠是非常活泼的金属,能与水发生剧烈反应,并放出气体,生成的溶液显碱性
(3)【实验探究】
实验一:把一小块擦干净的金属钠放到装有少量蒸馏水的试管中,点燃生成的气体,听到“噗”的一声后燃烧起来,说明有 气体生成
实验二:在剩余的溶液中滴加硫酸铜溶液,发现有蓝色沉淀
(4)【实验总结】实验一中发生反应的化学方程式是 ;实验二中发生反应的化学方程式是
(5)【实验拓展】兴趣小组又将一小块擦干净的金属钠放入盛有FeCl3溶液的烧杯中,观察到发生了化学反应,该反应的化学方程式是 .