根据下表回答问题:
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
|
溶解度 /g |
NaCl |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
NH4Cl |
33.5 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
|
(1)海水中含有大量的氯化钠,海水晒盐的原理是 ,氨碱法制纯碱先向饱和食盐水中通入氨气,通入氨气的作用是 ,可向滤出晶体后的NaHCO3溶液中加入 以回收氨,使之循环使用。
(2)氯化钠和氯化铵具有相同溶解度的温度范围在 ℃之间。
(3)图中,A是60℃时含有120g水的NH4Cl溶液,经过如下操作后,得到固体。

I.C中溶液的质量是 g.A溶液为NH4Cl的 (选填“饱和”或“不饱和”)溶液,该溶液中溶质的质量分数为 (结果精确到0.1%)。
II.对以上过程的分析,正确的是 (选填编号)。
①A到B的过程中,溶质质量没有改变
②B中溶质与溶剂的质量比为55.2:100
③由B到C开始析出NH4Cl固体的温度在40℃至50℃之间。
请结合如图所示实验回答问题。

(1)A实验中用玻璃棒搅拌的目的是 。
(2)B实验中错误操作造成的后果是 。
(3)C实验正、负极产生的气体体积比约为 。此实验说明水是由 组成的。
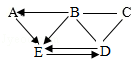
A~E为初中化学常见的五种不同类别的物质,其中A是通常状况下密度最小的气体,C广泛应用于玻璃、造纸纺织和洗涤剂的生产。它们之间的关系如图所示(“﹣”表示相邻两种物质能发生反应;“→”表示两种物质间的转化关系;图中部分反应物、生成物及反应条件已略去)。请回答下列问题:
(1)C的化学式是 。
(2)D的一种用途是 。
(3)A→E的化学方程式是 。
(4)B和D反应的基本反应类型是 。
金属在生活生产中有着非常广泛的应用,请回答下列问题。
(1)我国生产和使用铁器历史悠久,请写出工业用赤铁矿石炼铁的化学方程式: 。生铁和钢的性能不同,原因是 。
(2)铁在潮湿的空气中很容易生锈,请写出一种防止钢铁制品锈蚀的方法: 。
(3)向硝酸银和硝酸铜的混合溶液中加入一定量的锌粉,操作流程如图所示。

请回答:
①滤渣中一定含有的物质是 (填化学式,下同)。
②若滤液呈蓝色,滤液中一定含有的溶质是 。
能源、环境与人类的生活和社会发展密切相关。
(1)煤的使用在方便人们生活的同时,也对环境造成了不良影响,含硫煤不完全燃烧产生的气体污染物有 。因此应大力提倡使用新能源,下列不属于新能源的是 (填字母序号)。
A.太阳能 B.风能 C.石油
(2)乙醇汽油作为燃料的优点是 (答一点即可)。
(3)二甲醚( CH3OCH3)被认为是21世纪新型燃料,二甲醚在空气中充分燃烧生成二氧化碳和水,该反应的化学方程式是 。
某化学小组对石灰石灼烧后得到的固体进行相关探究。
成分分析
(1)检验灼烧过程中产生的新物质
①根据已有知识和经验判断:石灰石灼烧后固体中含有CaO,判断的依据是 (用化学方程式表示)。
②设计实验方案进行验证:
|
实验内容 |
实验现象 |
实验分析 |
|
取灼烧后固体放入盛有冷水的烧杯中,充分搅拌静置后,取少量上层澄清的液体置于试管中,向其中滴加2滴酚酞试液 |
溶液由无色变为 色 |
反应后生成碱,请写出该反应的化学方程式: |
(2)检验灼烧后固体中是否含有CaCO3
向盛有灼烧后固体的烧杯中滴加稀盐酸,有气泡产生,证明 。
数据分析
用反应前后质量差计算灼烧后固体中CaCO3的质量分数
化学小组设计以下两个实验方案,方案中反应前后质量差分别用m1与m2表示。(两方案中实验操作误差忽略不计,取用的灼烧后固体成分均匀、质量相等,固体中除CaO、CaCO3其余成分均不发生反应,所用稀盐酸经估算确保足量)
|
实验方案 |
数据测量 |
数据处理 |
|
|
反应前 |
反应后 |
反应前后质量差 |
|
|
方案一:取灼烧后固体放入烧杯中,加入稀盐酸充分反应,不再产生气泡 |
灼烧后固体的质量、所用稀盐酸质量 |
烧杯中剩余物质的质量 |
m1 |
|
方案二:取灼烧后固体继续灼烧,至固体的质量不再改变 |
灼烧后固体的质量 |
剩余固体的质量 |
m2 |
结合信息,比较m1与m2的关系。请写出两种不同猜想并分别说明理由。
猜想1及理由: 。
猜想2及理由: 。
经分析选择合理的实验方案,进行计算……
拓展研究
如图的酒精灯和酒精喷灯是常用的加热仪器,请回答下列问题:

(1)酒精灯是玻璃仪器,火焰温度通常可达300~500℃, (填“焰心“、“内焰”或“外焰”)温度最高。熄灭酒精灯的方法是 ,采用此方法灭火的原理是 。
(2)酒精喷灯一般是铜质仪器,火焰温度通常可达800﹣1000℃.使用酒精喷灯时应先向引火碗内注入 容量的酒精,用火柴将引火碗内酒精点燃,点燃引火碗内酒精的目的是 、 。