如图所示为实验室中常见气体制备、净化、干燥、收集和进行实验探究的部分仪器(组装实验装置时,可重复选择仪器),某化学小组的同学欲利用其进行下列各化学实验。

(1)以过氧化氢溶液为原料(二氧化锰作催化剂),在实验室中制备并收集干燥的氧气。按照要求设计实验装置,连接仪器,并检验装置的气密性。
①所选装置的连接顺序为 (从左至右填写装置序号字母)。
②制取氧气所发生反应的化学方程式为 。
③下列有关氧气制取和性质的叙述中,不正确的是 (填写序号A、B、C,D之一)
A.实验室制氧气时,应先加入药品,再检査装置的气密性
B.在此反应前后,二氧化锰的质量和化学性质都不发生改变
C.铁丝在纯氧中剧烈燃烧时,火星四射,生成黑色固体
D.氧气是一种化学性质比较活泼的气体
(2)用干燥纯净的氧气对纤维素的组成进行分析探究实验(资料显示纤维素只含C、H、O三种元素)。所选装置按"氧气→D→A→C→碱石灰干燥管"的顺序连接(实验前检验装置的气密性,假设所发生的化学反应都完全充分进行)。装置D的玻璃管中放入纤维素试样的质量为wg,充分反应后,测得装置A的质量增加ag,装置C的质量增加bg,则纤维素中碳元素的质量分数为 (计算结果用含字母的代数式表示)。
若实验中使用的氧气未干燥,这样测算出的纤维素中碳元素与氢元素的质量比与实际值比较将 (填"偏大""偏小""基本一致""无法确定"之一)
(3)用一氧化碳气体(含有少量二氧化碳和水蒸气)测定某铁的氧化物(Fe xO y)试样的元素组成比例,所选装置按"混合气体→A 1→D→C→A 2"的顺序连接(A 1、A 2为浓硫酸洗气瓶,实验前检验装置的气密性,假设所发生的化学反应都充分反应)。进行实验并记录实验数据,如下表所示:
装置编号 |
A 1中浓硫酸 |
D中玻璃管内固体 |
C中溶液 |
反应前质量 |
150g |
14.4g |
200g |
反应后质量 |
152.7g |
11.2g |
213.2g |
①请选择合理数据计算Fe xO y中x:y= (填写最简整数比)。
②从环保角度考虑,该实验方案设计还存在不完善之处,你的具体改进方案是 。
甲、乙、丙三个实验小组分别利用2g铜粉"测定空气中氧气的含量",实验装置见图。课外兴趣小组为研究实验中铜粉的氧化情况,又进行以下实验:
①兴趣小组将甲、乙、丙三个实验小组硬质玻璃管中的残留固体全部取出,称量后,置于烧杯中;
②在烧杯中加入足量稀硫酸使之充分反应,将剩余固体过滤、洗涤、干燥、称量;相关数据见下表:
|
甲组 |
乙组 |
丙组 |
|
|
反应前固体质量 |
2.016g |
2.016g |
2.024g |
|
反应后固体质量 |
1.936g |
1.936g |
1.904g |
(1)烧杯中发生反应的化学方程式为 ;
(2)甲、乙两组实验数据相同,残留固体中氧化铜的质量为 ,丙组残留固体中氧化铜的质量为 。
(3)兴趣小组通过分析数据得出:甲、乙两组实验数据更接近实际空气中氧气的含量,丙组差异较大。你认为丙组在"测定空气中氧气的含量"实验中,可能存在的操作失误是 。

白铜(Cu﹣Ni)是工业上常用的一种合金,金属镍(Ni)的金属活泼性与铁相似,且化合价显+2价。为测定20g某白铜样品中镍的质量,设计了如下实验:

试问:
(1)将白铜研碎的目的是 。
(2)白铜样品中镍的质量 g。
(3)所用稀硫酸中溶质的质量分数(写出计算过程)。
84消毒液是一种无色或者淡黄色具有刺激性气味的含氯消毒剂,有效成分为次氯酸钠(NaClO)。广泛用于医院、宾馆、旅游、家庭等的卫生消毒。某化学兴趣小组对该消毒液进行了如下系列探究。
【查阅资料】
Ⅰ84消毒液不稳定,其杀菌作用主要依靠有效氯,有效氯越高杀菌效果越好。
Ⅱ消毒杀菌就是使病毒蛋白质变性,鸡蛋中蛋白质发生变性反应时变成白色固体。
探究一:84消毒液中有效氯含量的稳定性
0.5%的84消毒液在不同温度、不同存放时间下的有效氯含量:
|
存放时间 (小时) |
不同温度下,有效氯存留率 |
|||
|
60℃ |
70℃ |
80℃ |
90℃ |
|
|
0(对照) |
100% |
100% |
100% |
100% |
|
3.0 |
…… |
…… |
94.66% |
88.05% |
|
6.0 |
…… |
96.66% |
89.67% |
74.69% |
|
12.0 |
…… |
93.32% |
82.62% |
…… |
|
20.0 |
94.75% |
…… |
…… |
…… |
|
20.0 |
92.99% |
…… |
…… |
…… |
【解释与结论】
(1)次氯酸钠(NaClO)中Cl元素的化合价为 。
(2)综合分析探究一中数据,在其他条件不变时,0.5%的84消毒液有效氯存留率受温度和时间的影响,其影响的变化趋势是 ,因此保存84消毒液应注意的问题是 。
探究二:不同浓度84消毒液的杀菌效果
在四只试管中各加入鸡蛋液2mL,分别加入不同浓度的消毒液,静置15分钟后,记录如下:
|
序号 |
2﹣1 |
2﹣2 |
2﹣3 |
2﹣4 |
|
实验操作 |
加入0.5mL消毒原液 |
加入0.5mL清毒 原液,12.5mL水 |
加入0.5mL消毒原液,50mL水 |
加入0.5mL消毒原液,100mL水 |
|
现象 |
液体表面产生气泡,无其他现象 |
液体中产生大量白色固体 |
液体中产生少量白色固体 |
液体中产生极少量白色固体 |
【解释与结论】
(3)探究二中杀菌效果最好的一组实验为 (填序号)。
(4)洁厕灵主要成分是盐酸,与84消毒液混合会产生有毒气体Cl 2,完成反应的化学方程式:2HCl+NaClO═Cl 2↑+H 2O+ 。
某兴趣小组在实验室发现盛有固体氢氧化钠的试剂瓶破裂瓶盖处有"白毛"状物质(如图),根据所学知识,他们推断"白毛"状固体物质中含有碳酸钠,依据是 。他们取5g白色固体,加水配成20g溶液倒入烧杯中,将40g氯化钡溶液分成四等份,分4次加入烧杯中,充分反应后测得数据如下表:
|
实验次数 |
1 |
2 |
3 |
4 |
|
加入氯化钡溶液的质量/g |
10 |
10 |
10 |
10 |
|
烧杯中所得溶液的质量/g |
28.03 |
36.06 |
44.09 |
54.09 |
(1)第 次实验,加入的氯化钡与碳酸钠恰好完全反应。
(2)求5g白色固体中碳酸钠的质量。(写出计算过程,结果保留两位小数)

化学是一门以实验为基础的自然科学。根据所学知识回答以下问题:
(1)实验室制取二氧化碳,应选用以下药品①块状石灰石②碳酸钠粉末③稀盐酸④稀硫酸中的 (填序号)。现有大理石粉末和稀硫酸,你认为 (填“能”或“否”)用于实验室制取二氧化碳。
(2)实验室有如图1装置,根据要求回答问题:
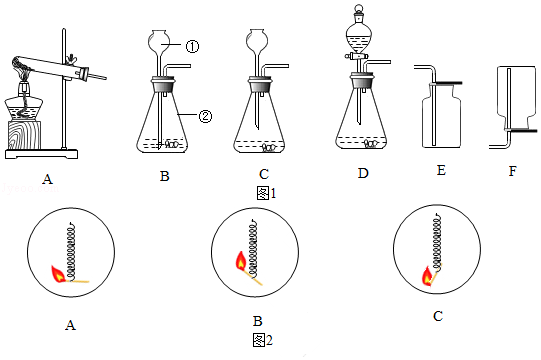
Ⅰ.写出标号仪器的名称① ,② 。
Ⅱ.对比装置B、C,有错误的是 (填序号,下同)。
Ⅲ.实验室要制取二氧化碳应选择的发生装置是 ,收集装置是 ;利用制取二氧化碳的发生和收集装置还能制取另外一种常见气体,利用此装置制取该气体的化学方程式是 。
Ⅳ.图2是同学们进行“铁丝在氧气中燃烧的性质实验”时的几种操作方式,更能提高实验成功率的方式是 (填序号)。
(3)有的同学完成上述实验后,提出“铁丝能否在二氧化碳中燃烧呢?”,他们设计了如下方案:(已知:在点燃的条件下,镁带能在二氧化碳中剧烈燃烧。)
方案①:将弯成螺旋状的细铁丝系上一根火柴,点燃火柴,待火柴快燃尽时,插入装有二氧化碳的集气瓶中,观察铁丝能否被引燃。
方案②:将弯成螺旋状的细铁丝系上一段镁带,点燃镁带,待镁带快燃尽时,插入装有二氧化碳的集气瓶中,观察铁丝能否被引燃。
你认为方案 (填①或②)更为科学,理由是 。