某化学小组从理论上初步探究"已知质量比的硝酸钾和氯化钠的混合物中提纯硝酸钾"。
【分析提纯方法】
表一:常温下(20℃)溶解度和溶解性的关系
溶解度S |
S≥10g |
1g≤S<10g |
0.01g≤S<1g |
S<0.01g |
溶解性 |
易溶 |
可溶 |
微溶 |
难溶 |
表二:硝酸钾和氯化钠在不同温度时的溶解度
温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
|
溶解度/g |
KNO 3 |
13.3 |
31.6 |
63.9 |
110 |
169 |
246 |
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
39.8 |
|
(1)常温下,KNO 3和NaCl的溶解性均为 。
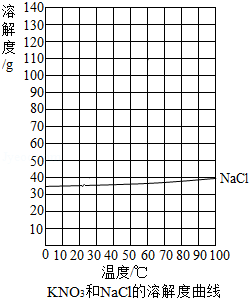
(2)根据表中数据,绘制KNO 3的溶解度曲线。
(3)根据KNO 3的溶解度曲线,获得KNO 3在70℃时的溶解度约为 g。
【设计提纯步骤】
(1)选取样品(95gKNO 3和5gNaCl的混合物)
(2)配制80℃时KNO 3的饱和溶液(加水约56.2mL,水的密度约为1g•mL ﹣ 1)
(3)降温至20℃
(4)得到晶体
【设计提纯方案】
为了证明(4)中得到的晶体为纯净的KNO 3,该小组同学结合已有知识,从理论上初步设计了以下方案;(不考虑不同溶质对溶解度的相互影响及实验过程中水和固体的损失等影响因素)
方案一 通过化学实验进行检验,取少量(4)中得到的晶体于试管中,加水配成溶液,滴加 ,观察实验现象。
方案二 计算析出KNO 3晶体的质量约为 g(精确到0.1g)与(4)中得到晶体的质量进行比较
方案三 与95%进行比较。
方案四 。
根据表中信息,请回答下列问题。
|
测试类别 S化合价 |
氢化物 |
单质 |
① |
酸 |
盐 |
|
+6 |
﹣ |
﹣ |
SO 3 |
H 2SO 4 |
Na 2SO 4CuSO 4FeSO 4(NH 4) 2SO 4 |
|
② |
﹣ |
﹣ |
SO 2 |
H 2SO 3 |
Na 2SO 3 |
|
0 |
﹣ |
S |
﹣ |
||
|
﹣2 |
H 2S |
﹣ |
﹣ |
H 2S |
Na 2S |
(1)填写表中内容:① ;② 。
(2)物质可以按照一定规律发生转化,请按要求各写出一个对应的化学方程式。
①置换反应 ;②复分解反应 。
(3)(NH 4) 2SO 4是农业上常用的铵态氮肥,在实验室检验其为铵态氮肥的实验操作是______(写出一种即可)
(4)2H 2S+SO 2═2S+2H 2O,反应前后硫元素化合价发生的变化是
(5)在实验室中,可用热的碱液除去试管内壁上附着的硫,请完成该反应的化学方程式: S+ NaOH═ Na 2SO 3+ + H 2O。
图1是某兴趣小组在学习碱的性质时进行的探究活动,请要求回答问题。
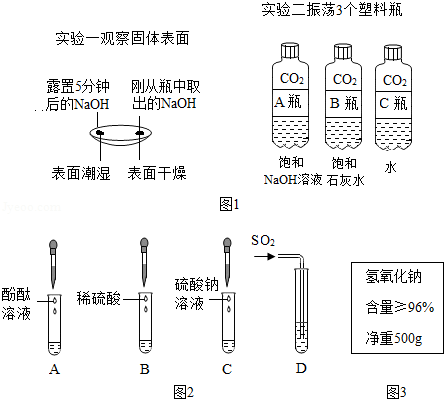
(1)通过分析实验一可知,氢氧化钠会吸收空气中的 。
(2)实验二中观察到3个塑料瓶变瘪的程度为A>B>C,可证明CO2能与NaOH、Ca(OH)2反应,其中C瓶在实验中起 作用。
(3)晓晓查阅资料了解到往Ba(OH)2溶液中滴加或通入下列图2中物质会产生如下现象:A中溶液显红色,B、C、D中均产生白色沉淀。
①写出D试管中反应的化学方程式 。
②不同的碱溶液中都含有OH﹣,所以,碱有一些相似的化学性质。上述关于Ba(OH)2性质的实验不能体现碱的相似性质的是 (填字母序号)
(4)冬冬发现工业上使用的氢氧化钠固体标签如图3所示,于是对其所含杂质进行了探究。
【提出问题】
【提出猜想】
猜想I:查阅资料可知,工业用氢氧化钠可能含有NaCl。
猜想Ⅱ:工业用氢氧化钠可能含有Na2CO3,原因是 (用简洁的文字表述)。
【进行实验】
|
实验步骤 |
实验现象 |
解释或结论 |
|
①取适量固体样品于试管中,加水溶解 |
固体全部溶解 |
/ |
|
②向①所得溶液中滴加过量的 |
一开始无明显变化,一会儿后产生能使澄清石灰水变浑浊的气体 |
样品中含有Na2CO3 |
|
③向②所得溶液中滴加几滴硝酸银溶液 |
产生白色沉淀 |
样品中还含有NaCl.反应的化学方程式为 |
根据如图回答问题。

(1)A中集气瓶内水的作用是 。
(2)B中集气瓶内水位最终约在刻度 处。
(3)C中制备氧气的化学方程式是 。
(4)D中若加入的固体是NH 4NO 3,实验现象是 。
(5)E中探究可燃物燃烧的条件之一是 。
A、B、C、D、E分别表示初中化学常见的五种物质,它们的部分反应和转化关系如图所示("﹣"表示两种物质能发生反应,"→"表示一种物质能转化成另一种物质,且省略部分反应物或生成物及条件),已知其中只有两种物质是氧化物,E是含有三种元素的物质。
(1)若D为水时,且A、B两物质能发生化合反应,请回答:
①写出A、E物质的化学式:A 、E ;
②A与B发生反应的现象为 。
(2)若D为二氧化碳时,请回答:
①写出A、C物质的化学式:A 、C ;
②按照图示所标明的物质关系,写出能生成空气污染物的化学反应方程式 。

如图是氢气和氧气发生反应的微观模拟图,请回答下列问题:
(1)在B图中将相关粒子图形补充完整;
(2)A图所示物质属于 (填物质分类),从微观角度说明理由是 ;
(3)画出比氧元素多一个周期少一个族的元素的原子结构示意图 .
