某同学设计如下几组实验,探究某些酸、碱、盐之间的复分解反应能否发生。
已知:BaSO4是白色固体,难溶于水,也不与盐酸反应。
【第一组】选取5种溶液,如图所示进行实验。
实验 |
现象及结论 |
解释 |
|
试管A和B中无明显现 象,不能确定反应是否 发生。 |
/ |
(1)试管C中产生 (填实验现象)。复分解反应已发生。 |
(2)试管C中减少的微粒是 (填微粒符号) |
|
试管D中有白色沉淀产生。复分解反应已发生。 |
(3)反应的化学方程式为 |
【第二组】对试管A和B中是否发生反应再探究,如图所示进行实验。
实验 |
现象及结论 |
解释 |
|
试管E中,滴加酚酞试液 后,溶液由无色变为红色; 滴加一定量稀硫酸后,溶 液由红色变为无色。 复分解反应已发生。 |
(4)从微观粒子变化的角 度分析试管E中反应的实 质是 。 |
试管F中始终无明显现象, 不能确定反应是否发生。 |
/ |
【第三组】对试管B中是否发生反应继续探究,如图所示进行实验。
实验 |
现象及结论 |
解释 |
|
试管G中溶液变红 |
(5)该实验的目的是为了检验试管G的溶液中存在 (填微粒符号)。 |
(6)向试管H中滴加 (填“试剂X”的化学式)溶液后,有白色 沉淀产生。 |
溶液中有SO42﹣存在。 |
|
结论 |
NaCl溶液与稀硫酸不发生复分解反应。 |
|
炼铁产生的废渣中含有大量
及少量铁和铁的化合物,工业上以该废渣为原料生产
的流程图如下:
(1)操作1:粉碎。粉碎的目的是;
(2)操作2:焙烧。高温条件下,通入空气,
和
反应生成了
和
,化学方程式为;
(3)操作3:(填操作名称);
(4)流程图中能循环利用的物质是。
江西不仅山清水秀、景色迷人,特色美食更是遍布各地,令各路“吃货”流连忘返。
(1)南昌“藜蒿炒腊肉”风味独特,清香扑鼻。从分子角度解释“清香扑鼻”的原因是:;
(2)赣州“斋婆柚”汁多味美,齿颊生津。柚子皮还可以吸附室内异味,写出一种具有同样性质的化学物质的名称;
(3)吉安“安福火腿”营养丰富,历史悠久。“火腿”中能为人体提供能量的一种营养素是 _____________;
(4)宜春“丰城冻米糖”松脆香甜,誉满江南。“冻米糖”中蔗糖的化学式为C12H22O11,其中氢元素和氧元素的质量比为;
(5)九江“茶饼”酥香可口,茶食精点。“茶饼”中所含锌元素的部分信息如下图,则下列说法正确的是__________(填序号)。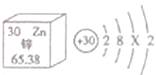
| A.锌的相对原子质量为65.38g |
| B.锌原子结构示意图中X为8 |
| C.锌原子在反应中容易得到电子 |
| D.锌原子核内质子数为30 |
《奔跑吧 兄弟》是一档热播的娱乐节目,其中蕴含着许多化学知识。
(1)节目最刺激的游戏是"撕名牌"。"名牌"是贴在队员衣服后面,标有自己姓名的标牌,制作材料有棉布、塑料等。塑料属于(填"有机化合物"或"无机化合物");鉴别棉布和涤纶布的方法是;
(2)其中一期节目,队员用水枪将酚酞溶液喷射到对方的"名牌"上,立即变红色。事先浸泡"名牌"的溶液可能是;
(3)另一期节目,蓝色的"污水"中注入"神秘水"后立即变得澄清透明。"污水"是单宁酸和硫酸亚铁溶液混合后发生一系列化学反应形成的,加入无色的"神秘水"草酸后,污水变澄清。其中的一个反应为
,则
的化学式为;草酸(
)中碳元素的化合价为。
| A. | 白酒 | B. | 柠檬酸 |
| C. | 食盐溶液 | D. | 纯碱溶液 |
根据下图某牙膏商标上的部分文字,用化学用语填空
(1)图中一种金属元素的符号。
(2)二氧化硅的化学式。
(3)
个硝酸根离子的符号。
下图是两种物质的溶解度曲线,下列说法正确的是()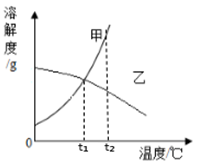
| A. | 甲的溶解度大于乙的溶解度 |
| B. | ℃时等质量甲、乙两种物质的饱和溶液中溶质质量相等 |
| C. | ℃时等质量的甲、乙两物质的饱和溶液降温至 ℃时,两溶液中溶质质量分数相等 |
| D. | 氧气的溶解度随温度变化的规律与图中乙相似 |