几种物质在不同温度时的溶解度如下表所示:
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
|
溶解度 /g |
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
37.8 |
38.4 |
KCl |
27.6 |
31.0 |
34.0 |
34.7 |
40.0 |
42.6 |
45.5 |
48.3 |
51.1 |
|
NH4Cl |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
60.2 |
65.6 |
|
KNO3 |
14.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
169 |
|
请回答下列问题:
(1)20℃时,上述四种物质中溶解度最大的是 (填化学式,下同)。
(2)将温度为80℃、质量相同的上述四种物质的饱和溶液分别降温到20℃,析出 晶题体最多的是 。
(3)在某温度范围内NaCl和KCl的溶解度可能相等,该温度范围是 (填字母序号)。
A.10℃~20℃
B.20℃~30℃
C.30℃~40℃
D.40℃~50℃
(4)20℃时将20 gNaCl加入50g水中,充分溶解后所得溶液中溶质的质量分数是 (计算结果精确至 0.1%)。
蒸馏是净化水的方法之一,下图是实验室常用的蒸馏装置,回答下列问题:
(1)用酒精灯加热时要用其(填“外焰”、“内焰”或“焰心”)进行加热。
(2)蒸馏烧瓶中自来水的体积不超过其体积的,烧瓶中碎瓷片的作用是。
(3)冷却水从冷凝管的(填“a”或“b”)口进入。
(4)蒸馏后收集到的蒸馏水是(填“纯净物”或“混合物”)。
(5)自制的简易净水器常常用到活性炭,主要是利用其具有性。
尿素[(NH2)2CO]是农业上重要的氮肥。工业上合成尿素的工艺流程如下: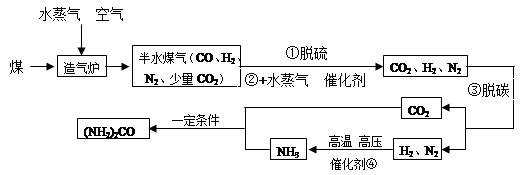
(1)煤是我国目前主要的化石燃料,主要含有。
(2)造气炉中发生反应:C + H2O CO + H2,C + O2
CO + H2,C + O2 CO2,上述两个反应中表现还原性的物质是(填化学式)。
CO2,上述两个反应中表现还原性的物质是(填化学式)。
(3)脱碳过程③是通过一定的工艺流程将CO2与H2、N2分离,此过程发生的是(填“物理变化”或“化学变化”)。
(4)反应④的基本类型是。
(5)写出由CO2和NH3合成尿素[(NH2)2CO]并生成水的反应方程式。
水是人类宝贵的自然资源,1993年1月18日,第四十七届联合国大会作出决议,确定每年的3月22日为“世界水日”。根据所学知识回答:
(1)电解水实验时正极放出的气体是,该实验证明分子是的(填“可分”或“不可分”)。
(2)水(H2O)和过氧化氢(H2O2)都是由氢元素、氧元素组成,它们的化学性质(填“相同”或“不同”),水用来灭火是因为。
(3)下列水的净化程度相对较高的是(填编号)。
| A.静置沉淀 | B.吸附沉淀 | C.蒸馏 | D.过滤 |
(4)硬水中含有较多可溶性钙镁离子的化合物,实验室或日常生活中通常向一定量的水中滴加的方法来检验硬水和软水。
人们使用的燃料大多来自化石燃料,天然气是化石燃料之一,其主要成分是甲烷。根据所学知识回答:
(1)点燃甲烷前一定要验纯。验纯方法是:,如果听到,证明甲烷不纯。
(2)若甲烷中含有少量的二氧化碳,除去二氧化碳的反应方程式是。
(3)甲烷和甲醇燃烧的产物都是二氧化碳和水,由此可以确定两种物质中含有的元素是
,除此之外甲醇组成中可能含有的元素是。
图①~③是三种微粒的结构示意图,图④是氧元素在周期表中的相关信息。
根据所学知识回答:
(1)图①表示的是元素(填“金属”、“非金属”或“稀有气体”),该元素形成的单质在空气中所占的体积分数大约是。
(2)图②和图③表示的是(填“同种”或“不同种”)元素,其中图②表示的微粒符号是(用元素符号表示)。
(3)由图④所给信息可知氧元素的原子核外电子数是,氧元素与图③表示的元素形成化合物的化学式是。