A、B、C为初中科学常见的三种无机物,它们之间有如图所示的转化关系("→"表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物及反应条件已略去)。请回答:
(1)若C是气体,它能使带火星的木条复燃,A、B所属的物质类别和组成元素都相同,则A→B的化学方程式为 ;
(2)若A为光合作用的原料之一,A与B属于不同物质类别,B和C属于同种物质类别,A、B、C三种物质中都含有相同的两种元素,则C可能的物质类别是 。

实验室制取气体所需装置如下图所示。 
A B C D E
请回答以下问题:
(1)装置中标“a”的仪器名称是_____。
(2)用高锰酸钾制取氧气时,反应的化学方程式为_____,所选用的制取装置是_____(填字母序号,下同)。
(3)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是_____,反应的化学方程式为_____。该装置还可用于制氧气,反应的化学方程式为_____。
下列用字母表示的七种物质都是由氢、碳、氧、钠、氯、钙等元素组成的化合物,均为初中化学常见物质。
(1)A、B、C都是氧化物。A与B反应的产物可以使紫色石蕊溶液变成红色,B与C化合后的产物D微溶于水,则A的化学式是,B与C反应的化学方程式是。
(2)E是天然气的主要成分,是一种比较清洁的燃料。E在氧气中燃烧可生成A和B,则E
燃烧的化学方程式为。
(3)F在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产,F与G反应的生成物中也有
A和B, 则F与G反应的化学方程式是。
(4)D可中和某些工厂污水中含有的G,D与G反应的化学方程式为。
(5)D与F固体混合物溶于水后发生化学反应,写出所得溶液中溶质的所有可能组成
(填化学式)。
(6分) 水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)下图实验中,当试管1中气体的体积为6mL时,试管2中气体体积约为mL,发生反应的化学方程式为________。
(2)水常用来配制各种溶液,硝酸钾溶液中的溶质为________。
(3)农业生产常用溶质的质量分数为10% ~ 20%的NaCl溶液来选种。现将300 g 25%的NaCl溶液稀释为15%的NaCl溶液,需要加水的质量为________g。
(4)根据下表回答问题。
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
|
| 溶解度 /g |
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
39.8 |
| NH4Cl |
29.4 |
37.2 |
45.8 |
55.2 |
65.6 |
77.3 |
① 60 ℃时,向两个分别盛有50 g NaCl和NH4Cl的烧杯中,各加入100 g的水,充分溶解后,为饱和溶液的是________溶液。
② 将上述实验后的两个烧杯均降温至40℃。下列说法中,正确的是________(填字母序号)。
A.两个烧杯中的溶液均为饱和溶液
B.两个烧杯中溶液的质量都可能不变
C.两个烧杯中溶液的质量减小的一样多
D.两个烧杯中溶质的质量分数都一定减小
能源、环境与人类的生活和社会发展密切相关。
(1)目前,人类以化石燃料为主要能源。常见的化石燃料包括煤、石油和。
(2)为减少污染、提高煤的利用率,可将其转化为可燃性气体,此过程可认为是碳与水的反应,其微观示意图如下所示:
① 该反应的化学方程式为。
② 该反应生成物的分子个数比为。
(3)为减少温室气体排放,人们积极寻找不含碳元素的燃料。经研究发现NH3燃烧的产物没有污染,且释放大量能量,有一定应用前景。
① NH3中氮元素和氢元素的质量比为。
② 将NH3燃烧反应的化学方程式补充完整:4NH3 + 3O2 点燃 6H2O + 。
钠的化合物在日常生活中应用广泛。
(1)在元素周期表中,钠元素的信息如图所示,钠元素的相对原子质量为_____。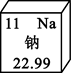
(2)氢氧化钠可用于制杀虫剂,氢氧化钠的俗名是_____(写一种)。
(3)次氯酸钠(NaClO)是84消毒液的有效成分,次氯酸钠中氯元素的化合价为_____。
(4)碳酸氢钠是发酵粉的主要成分,碳酸氢钠与盐酸反应的化学方程式为_________。
(5)氨基钠(NaNH2)是合成维生素A的原料。工业上生产氨基钠的化学反应方程式为
2Na + 2NH3△2NaNH2 + H2↑,该反应属于基本反应类型中的_______反应。