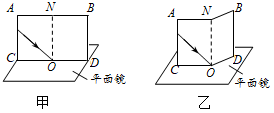
“探究光的反射规律”的实验装置如图甲所示,平面镜放在水平桌面上,标有刻度(图中未画出)的白色纸板ABCD能绕垂直于CD的ON轴翻转,在纸板上安装一支可在纸板平面内自由移动的激光笔。
(1)实验前,应将纸板 放置平面镜上;移动激光笔,使入射光束绕入射点O沿逆时针方向转动,可观察到反射光束沿 时针方向转动;
(2)移动激光笔,使入射角为45°,测得反射角也为45°,由此就得出“光反射时,反射角等于入射角”的结论你认为有何不妥之处? ;
(3)如图乙所示,将纸板右半部分绕ON向后翻转任意角度,发现纸板上均无反射光束呈现此现象说明了: ;
(4)在图甲中,若将纸板(连同激光笔)绕CD向后倾斜,此时反射光束 (选填字母符号)。
A.仍在纸板上呈现
B.被纸板挡住
C.在纸板前方
(5)实验结束后,同组的小明和小刚都想从镜子中看到对方的眼睛,而不想让对方看到自己的眼睛,结果他俩谁都没有能做到,你认为没有能做到的原因是 。
在测2.5V小灯泡(电阻大约为10Ω左右)额定功率的实验时,小明连接了如图甲所示的电路,其中电源电压为6V。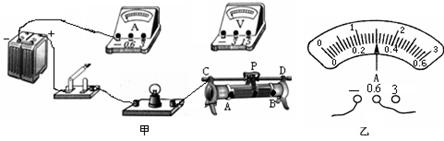
(1)在连接电路时,开关必须。请将实物电路连接完整(要求:滑动变阻器的滑片向右移动时小灯变亮)。
(2)若在连接电路时,有A (10Ω 1A)和B (20Ω 1A)两个滑动变阻器可供选择,则应该选择变阻器
(填“A”或“B”)连入电路,才能保证实验顺利进行。
(3)小明合理地连接好电路,闭合开关,发现无论怎样调节滑动变阻器灯泡都不亮。小明分析后发现是灯泡的故障。请你依据表一中电流表、电压表示数出现的几种情况,帮小明判断故障原因,并将其填写在表一对应的空格中。
(4)排除故障后,小明调节变阻器滑片的位置,使小灯泡两端电压分别为2V、2.5V、2.8V,依次测出通过小灯泡的电流,并观察发光情况,记录在表二中.当小灯泡正常发光时,电流表示数如图乙所示,此时小灯泡电阻是Ω(计算结果保留两位小数),小灯泡的额定功率是W。
小明和小丽利用如图所示的装置探究“导体产生的热量与电阻大小的关系” 。
(1)如图所示,质量相等的两瓶煤油中都浸泡着一段材料与长度均相同的金属丝,已知甲电阻比较小,则两根金属丝中横截面积较大的是(选填“甲”或“乙”)。
(2)实验中,小明和小丽发现烧瓶中温度计的示数升高较快.这表明:在和
相同的情况下,导体的电阻越,产生的热量越多。
(3)小明提议利用该装置改做“比较水和煤油比热容的大小”的实验,则他们应将其中一烧瓶中的煤油换成相等的水,并使甲、乙两烧瓶中金属丝的电阻。水和煤油吸热的多少是通过
来反映的(选填“温度计示数”或“加热时间”)。
(4)这两个实验中除运用了控制变量的研究方法外,还用到的研究方法是( )
| A.类比法 | B.替代法 | C.转换法 | D.建模法 |
如图是测定滑轮组机械效率的实验装置,小明测量的有关数据如下表所示:
| 次数 |
钩码重 G/N |
钩码上升的高度h/m |
拉力 F/N |
细线自由端移动的距离s/m |
机械效率 η/% |
| 1 |
2.0 |
0. 03 |
1.6 |
0.06 |
|
| 2 |
3.0 |
0.05 |
0.1 |
75 |
(1)请你根据表中数据在图中画出实验时滑轮组的绕线情况,并补全表中的空格。
(2)若提升的钩码重增加到6N,则该滑轮组的机械效率将(填“变大”、“变小”或“不变”)。
(3)小明在实验过程中,应当拉动弹簧测力计,才能使弹簧测力计的示数保持稳定。
某同学做探究杠杆平衡条件的实验,实验前发现杠杆左端低,右端高,应将左侧的平衡螺母向
(选填“左”或“右”)调节,使杠杆在水平位置平衡这样做的目的是为了便于测量;实验时,在A点悬挂2个重均为0.5N的钩码(如图示),在B点用弹簧测力计拉杠杆,使其水平平衡。要使弹簧测力计示数最小,弹簧测力计的拉力应沿方向,大小为N。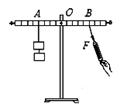
在测定“小灯泡额定电功率”的实验中,已知小灯泡的额定电压为2.5V.
(1)请你用笔画线代替导线,将图甲的实物电路连接完整。
(2)实验时,电源电压为6V,小灯泡的电阻大约为10Ω.滑动变阻器有“10( 2A”和“20( 1A”两种供你选择,应该选择_______的滑动变阻器.
(3)闭合开关后,移动滑动变阻器的滑片,当观察到电压表的示数为_______V时,小灯泡正常发光,此时电流表的示数如图乙所示,则该灯泡的额定功率为_______ W .
(4)有些同学提出,利用上面的实验器材,在不改变电路连接的情况下还可以探究“电流与电压的关系”,你认为这种说法正确吗?请简述原因:_________________________