某班同学用氢氧化钠溶液和稀硫酸进行中和反应实验。
(1)甲同学在烧杯中加入约5mL氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈 色,接着用滴管滴入一定量的稀硫酸,再用玻璃棒搅拌,发现溶液变为无色,该反应的化学方程式为 。
(2)甲、乙、丙同学对反应后溶液中的溶质成分进行探究。
[猜想与假设]反应后溶液中的溶质是什么?
猜想一:只Na 2SO 4
猜想二:
猜想三:Na 2SO 4和NaOH
以上猜想中,可以直接排除的是 ,理由 。
[实验探究]
为了验证另外两种猜想,甲、乙、丙同学设计如下实验方案:
实验操作 |
实验现象 |
实验结论 |
|
甲同学方案 |
取少量反应后的溶液于试管中,向试管中滴加BaCl 2溶液 |
白色沉淀产生 |
猜想二成立 |
乙同学方案 |
取少量反应后的溶液于试管中,向试管中加入 |
气泡产生 |
猜想二成立 |
丙同学方案 |
取少量反应后的溶液于试管中,向试管中加入生锈的铁钉 |
|
猜想二成立 |
老师认为甲同学方案不合理,你认为理由是 。
[反思交流]实验结束后,废液处理方法正确的是 (填序号)。
A.倒入下水道
B.倒入废液缸
C.带出实验室
学习了金属的有关知识后,同学们知道了如何鉴别黄金和黄铜(铜锌合金,俗名“愚人金”)。某化学兴趣小组的同学为了进一步测定某黄铜的组成,称取了黄铜样品50g放入锥形瓶中,向其中分5次共加入250g稀硫酸,测得数据记录如下表。
|
次数 质量 |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
|
累计加入稀硫酸的质量/g |
50 |
100 |
150 |
200 |
250 |
|
累计产生气体的质量/g |
0.2 |
x |
0.6 |
0.7 |
0.7 |
回答下列问题:
(1)x= ,该样品中铜的质量为 g。
(2)请在如图中画出样品中加入250g稀硫酸,产生气体的质量与稀硫酸的质量变化关系示意图。

(3)黄铜样品与稀硫酸恰好完全反应时,所得溶液的溶质的质量分数是多少?(精确到0.01)
工业上用闪锌矿(主要含ZnS,还含PbS等杂质)制备锌的流程如图1(部分产物略去):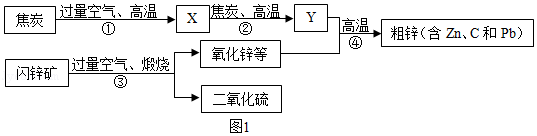
(1)X的化学式是 ,图1中用过量空气的目的是 。
(2)①~④中属于化合反应的是 。
(3)Zn (填“能”或“不能”)与PbCl2溶被反应。
(4)写出反应③中生成ZnO的化学方程式 。
(5)结合下表数据设计:从粗锌中分离出纯锌的方案是 。
|
物质 |
Zn |
Pb |
C |
|
沸点℃ |
907 |
1749 |
4827 |
(6)反应②中固体质量随反应时间的变化图示如图,计算产生Y的质量。(写出必要的计算过程)

2017年5月,中国首次海城天然气水合物(可燃冰)试采成功,成为全球第一个稳定开采可燃冰的国家。可燃冰开采困难重重,原因之一是可然冰极不稳定易爆炸,大甲烷气体涌入大气层,会产生比二氧化碳更为严重的温室效应。置换法是开采方法之一,将CO2液化后进入1500米以下的洋面,就会生成二氧化碳水合物沉人海底,因CO2较甲烷易于形成水合物,因而就可能将甲烷水合物中的甲烷分子置换出来。
(1)甲烷属于 (填“有机物”或“无机物”),其氢元素的质量分数为 。
(2)甲烷燃烧是将化学能主要转化为 能,甲烷燃料电池则是将化学能转化为 能。
(3)下列有关说法正确的是 。
A.开采可燃冰不会产生环境问题 B.二氧化碳水合物的密度比水小
C.可燃冰比二氧化碳水合物稳定 D.可燃冰是一种前景广阔的清洁燃料
(4)可燃冰的微观构成为46个H2O分子形成8个笼,有6个笼中每个笼容纳了1个CH4分子,余下2个笼每个容纳1个H2O分子,则可燃冰中H2O与CH4的分子数之比是 。
(5)一定条件下,甲烷与二氧化碳反应是回收处理二氧化碳的一种方法,产物都是常见双(两)原子分子,请写出反应的化学方程式 。
地壳中的元素分布(质量分数)如图,请回答下列问题。

(1)元素X是 ,由X与Y组成的化合物的化学式是 。
(2)地壳中的赤铁矿(Fe2O3)与CO高温反应可炼铁,其中Fe2O3发生了 反应(填“氧化”或“还原”)。
(3)如图是Si与Cl2反应生成SiCl4的图示,请在方框内补充所缺反应物的图示。

某同学设计的工业制备氢氧化钠的流程如图
1.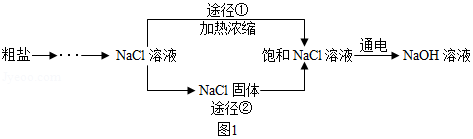
资料:2NaCl+2H2O 2NaOH+H2↑+C12↑,两电极,一端得到NaOH和H2,另一端得到Cl2。
2NaOH+H2↑+C12↑,两电极,一端得到NaOH和H2,另一端得到Cl2。
(1)晾晒海水得到粗盐的原理是
(2)实验室蒸发用到的仪器有铁架台(带铁圈)、坩埚钳、石棉网、酒精灯、玻璃棒和______
(3)工业生产中应选择途径 (“①”或“②”),理由是
(4)Cl2可用于生产84消毒液(有效成分 NaClO),反应原理为:Cl2+2NaOH=NaCl+NaClO+H2O,反应前后氯元素的化合价有 种。
(5)图2实验测定水组成,不能加入NaCl增强水的导电性的理由是 。电解水的化学方程式为 。
(6)图3实验获得84消毒液,直流电源正极应与 (填a或b)连接,才能使 NaClO的含量更高。