陈东同学在做“盐酸中和氢氧化钠”的实验时,实验前忘记向氢氧化钠溶液中滴加酚酞溶液,导致无法判断中和反应进行的程度,于是他对反应后溶液的酸碱性进行了探究。
[探究目的]确定反应后溶液的酸碱性
[猜想与假设]反应后溶液可能呈碱性,也可能呈 ,也可能呈 。
[实验验证]
实验操作 |
实验现象 |
实验结论 |
取反应后溶液少许,滴加几滴酚酞溶液 |
|
溶液呈酸性或中性 |
[继续验证]可以设计多种方案进行验证
实验操作 |
实验现象 |
实验结论 |
方案1:取反应后溶液少许,加入少量氧化铜粉末 |
若粉末部分或全部溶解,溶液变为蓝色 |
溶液呈 |
若粉末不溶解,溶液不变色 |
溶液呈 |
|
方案2:取反应后溶液少许,加入少量 |
若有气体放出,溶液变为浅绿色 |
溶液呈酸性,反应的化学方程式是 |
若 |
溶液呈中性 |
根据以下装置图,回答有关问题:
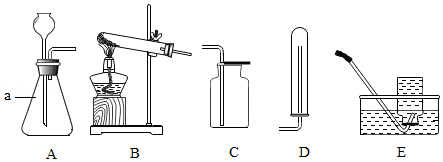
(1)写出图中标号为a的仪器名称 .
(2)实验室用氯酸钾制取氧气,化学方程式为 ,该反应的基本反应类型是 ,停止加热时应先将导管移出水面,其理由是 .
(3)用C装置收集氧气,验满的方法是 .
(4)实验室制取CO2应选择的发生和收集装置是 (填字母序号).
(5)用A装置制取气体时,长颈漏斗的下端管口要 ,以防止生成的气体逸出.
化学兴趣小组的同学在做完“二氧化碳的实验室制取“的实验后,对反应后废液中溶质的成分产生了兴趣并进行了以下探究:
(1)实验室制取二氧化碳的化学方程式为 ;
(2)[提出问题]:废液中的溶质含有哪些物质?
[猜想与假设]:猜想Ⅰ:溶液中的溶质只有氯化钙;
猜想Ⅱ:废液中的溶质有 .
[进行实验]
|
实验操作 |
实验现象 |
实验结论 |
|
取少量反应后的废液于试管中,向其中加入Na2CO3溶液至过量 |
只有 |
猜想Ⅰ正确 |
|
先 后 |
猜想Ⅱ正确 |
[反思拓展]:如果猜想Ⅱ正确,要使废液中只含有氯化钙,正确的处理方法是加入过量的 .
如图表示某些物质间的转化关系(反应条件和部分产物已省略).常温下A、C是由相同元素组成的无色液体,且C是一种最常用的溶剂;D、I、J均为无色气体,其中I能使澄清石灰水变浑浊;K为红棕色粉末.请回答下列问题:
(1)反应①中B物质的作用是 .
(2)写出图中反应⑤的化学方程式 .
(3)写出图中反应⑥的化学方程式 .

现有含杂质的氢氧化钙样品10g向其中加入10%的稀盐酸溶液73g恰好完全反应(杂质不参与反应),求样品中氢氧化钙的质量分数。
根据如图装置,结合所学化学知识回答下列问题

(1)写出标号仪器①的名称: 。
(2)实验室选择装置B用高锰酸钾制取氧气时,你认为B装置存在的问题是 ,该反应的化学方程式是 ,如果用排空气法收集氧气,则验满的方法是 。
(3)实验室制取CO 2可选择的发生装置是 (填字母),该反应的化学方程式为 。
(4)通常情况下,氨气(NH 3)是一种无色、有刺激性气味的有毒气体,密度比空气小,极易溶于水且水溶液显碱性。实验室里,用氢氧化钙固体和氯化铵固体反应制取氨气。实验室制取氨气选择的发生装置是 (填字母),若选择E装置收集氨气,气体应该从 (填"a"或"b")口进入。实验过程中多余的氨气用酸性溶液吸收,吸收的目的是 。